酵素の立体構造、「SACLA」のX線レーザーを用いて常温、原子分解能構造解析に成功
体内に近い環境での酵素反応機構解明から、新薬や機能性分子創生に期待
概要
桝田哲哉 農学研究科助教、岩田想 医学研究科教授(理化学研究所グループディレクター)、菅原道泰 理化学研究所特別研究員、鈴木守 大阪大学蛋白質研究所准教授、登野健介高輝度光科学研究センターチームリーダーらの共同研究グループは、X線自由電子レーザー(以下、XFEL:X-ray Free-Electron Laser)施設「SACLA」 を用いた「連続フェムト秒結晶構造解析(以下、SFX)」 という手法を使い、酵素の一種である「プロテイナーゼK」 の構造を原子分解能 での解析に成功しました。SFXを用いて原子分解能で構造決定した初めての成果です。今回の研究では、SACLAの高エネルギービーム特性を活かし「プロテイナーゼK」の1.20 Åの原子分解能での解析に成功しました。原子分解能による解析では、各原子を独立して見分けることができ、原子間の距離を正確に見積もることができます。また、水素原子の一部を可視化、窒素と酸素の原子種を区別することも可能です。また、今回の成果の特徴は解析を原子分解能かつ常温で行ったことにあります。凍結結晶の解析結果とは異なった、常温特有の「タンパク質側鎖や水分子の動き」を確認できたのは大きな進歩です。また非凍結結晶との比較でも、放射線による損傷のない構造が得られ、これまで見出されていなかった部位での「水分子の存在」が確認できました。本手法を用いた常温特有の「タンパク質や水の動き」、「酵素反応機構」が明らかとなることで、医薬品や機能性素材の設計開発など、医療や工業への幅広い応用も期待されます。本成果は、2017年3月31日に英国の科学雑誌Scientific Reportsに掲載されました。
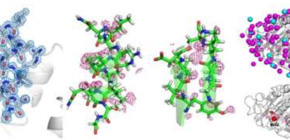
図1 今回明らかになった「プロテイナーゼK」の構造
研究の背景
X線自由電子レーザー(XFEL:X-ray Free-Electron Laser)は試料への照射時間が10 フェムト秒(1 フェムト秒は1,000兆分の1 秒)以下という超短時間のため、タンパク質が壊れる前の微結晶の回折イメージを検出できます。このX線レーザーの特性を利用したタンパク質の構造決定法として、「連続フェムト秒結晶構造解析(SFX)」が注目されています。SFXではインジェクター(噴出装置)から噴出させた多数の微小結晶を含む試料にXFELを照射し、各結晶からの回折イメージを連続的に収集します。SFXは常温で解析を行うことができるため、従来の低温条件下(100 K,-173 ℃)で行う実験とは異なり、生理条件(生体内)に近く、常温で放射線損傷の影響がない構造が得られることや、フェムト秒~ピコ秒の高い時間分解能で構造解析が可能であるという利点があります。
これまでSFXによる「創薬ターゲット蛋白質の迅速構造解析法の確立」課題を通し、2014年には、タンパク質結晶を高粘度物質のグリースに混ぜ、インジェクターからゆっくりと試料を押し出し、タンパク質結晶のX線回折実験を行うことができる「グリースマトリックス法」を開発しました。更に2016年にはグリースに替わる新しい輸送媒体(ヒアルロン酸)も見出しています。この手法確立により、常温で放射線損傷の影響がない構造データの収集、新規タンパク質の立体構造決定をはじめ、時分割解析によりタンパク質の動的構造変化を捉える研究がなされています。しかしながら、原子分解能での精度の高い構造解析には成功していませんでした。現在、XFEL解析施設として、米国のXFEL施設LCLSと日本のSACLAが稼働していますが、米国のLCLS施設に比べて、SACLAでは高エネルギーX線が使用可能である点が大きな特徴です。今回共同研究グループは、X線自由電子レーザー施設「SACLA」の高エネルギーX線(13 keV、ビームラインはBL3を使用)を用いた連続フェムト秒結晶構造解析によって、プロテイナーゼKという酵素の「現時点」では唯一の原子分解能構造解析に成功しました。
研究手法・成果
共同研究グループは、これまで「連続フェムト秒結晶構造解析(SFX)」において7 keVや10 keVのX線を用いて複数回以上の実験実績のある数種のタンパク質の中から、回折分解能が良好な「プロテイナーゼK」を選びました。プロテイナーゼKの微結晶(8-12 μm)をセルロース媒体と混合し、SACLAの優位点である高エネルギーX線(13 keV)を用いてSFX実験を行いました。実験の結果、82,000 枚の回折イメージを収集し、1.20 Åの分解能で構造決定を行うことができました。
この解析により、常温で、αヘリックスやβストランドなどタンパク質の2次構造を形成する部位の「水素原子」の可視化にも成功しました (図2) 。またSPring-8に於いて、凍結低温条件下での単結晶構造解析も行い、今回SFXで得られた構造と相違点があるか検討しました。活性部位の構造は比較的似ていましたが、近傍の水分子の配置が異なっていました (図3) 。また常温特有の「タンパク質側鎖の動き」も確認できました。非凍結結晶の解析結果との比較でも、これまで見出されていなかった部位での「水分子の存在」が今回明らかになりました (図4) 。
波及効果、今後の予定
高分解能結晶構造解析は放射線による試料の損傷を防ぐため、急速に結晶を凍結する手法やX線の照射位置を順次変えるような手法を用いて行われています。しかしながら、凍結処理を行うことにより結晶が収縮したり、モザイシティ(結晶内の配向の度合いを示す概念的な指標)が低下したりする現象や、タンパク質の活性部位に凍結に用いる抗凍結剤などが封入され機能を阻害する弊害なども知られています。また凍結に伴いタンパク質分子表面の水分子の配置やタンパク質の側鎖構造が変化し、タンパク質内部にも影響を及ぼすなどの事例も指摘されています。そのため人為的な影響が少なく、生理的な温度下での精度の高い構造情報が、タンパク質-リガンド間の精緻な相互作用解析に有益な知見を与えます。本成果で得られた技術や手法を用いて、常温特有のタンパク質や水分子の動き、酵素反応機構を明らかとすることで、医薬品や機能性素材の設計開発など、幅広い応用利用が期待されます。
研究プロジェクトについて
本研究は、文部科学省 X 線自由電子レーザー重点戦略研究課題「創薬ターゲット蛋白質の迅速構造解析法の開発」(研究代表者:岩田想)などの支援を受けて実施されました。
<論文タイトルと著者>
タイトル:Atomic resolution structure of serine protease proteinase K at ambient temperature
著者:Tetsuya Masuda, Mamoru Suzuki, Shigeyuki Inoue, Changyong Song, Takanori Nakane Eriko Nango, Rie Tanaka, Kensuke Tono, Yasumasa Joti, Takashi Kameshima, Takaki Hatsui, Makina Yabashi, Bunzo Mikami, Osamu Nureki, Keiji Numata, So Iwata & Michihiro Sugahara
掲載誌:Scientific Reports
参考図
図2 SFX で可視化できた水素原子
αヘリックス(a),βストランド(b),ターン構造(c)で常温において水素原子の一部に電子密度(ピンク色メッシュ:hydrogenomit map)が確認できた。
図3 プロテイナーゼKの活性部位
活性に係わるアミノ酸残基(Asp39, His69, Ser224;catalytic triad)の近傍を示す。(a)SFX構造における電子密度マップ:複数の水分子(W46, W123, W132)も確認できた。(b)放射光(SRX)凍結(Cryo)構造データとの比較:SFX(常温:灰色)と放射光凍結条件で測定した構造(SRX_cryo:シアン色)の比較。Asn161の側鎖の配置と水(W132)の配置が大きく異なっている。
図4 SFX と非凍結放射光SRX 構造との水分子の分布比較
常温の放射光で決定された構造SRX_2prk(a), SRX_4b5l(b)との比較。上段:SFX特有の水を紫色、SRX特有の水をシアン色で示す。下段:SFXとSRXで共通に存在している水の中で非常にフレキシブルな動き(温度因子が1.5倍以上高い値を示す)をする水を赤色で示す。ピンク色の残基は活性部位(Asp39, His69, Ser224;catalytic triad)を示す。
参考URL
大阪大学蛋白質研究所 鈴木守ユニット
http://www.protein.osaka-u.ac.jp/rcsfp/supracryst/suzuki/index.html
用語説明
- SACLA
理化学研究所と高輝度光科学研究センター(JASRI)による日本初のX線自由電子レーザー(XFEL:X-ray Free-Electron Laser)施設。SPring-8 Angstrom Compact free electron Laserの頭文字を取ってSACLAと命名された。加速器の中で電子の固まりを正確な制御の下で一斉に振動させ、0.1 ナノメートル以下という世界最短波長のX線レーザーを発振する。
- 連続フェムト秒結晶構造解析
多数の微結晶を含む液体などをインジェクターから噴出しながら、XFELを照射し結晶構造を解析する手法。配向の異なる多数の微小結晶からの回折データを連続的に収集する。
- プロテイナーゼK
ケラチンを消化する機能を有する酵素。分子生物学の領域では核酸精製の際によく用いられる。
- 原子分解能
原子間結合距離(1.20 Å)以下の分解能。各原子を独立して見分けることができる。
