細菌・ウイルス感染防御に必須の良質抗体産生を解明
転写因子「Foxo1」の働きに注目、ワクチン戦略のターゲットに!
本研究成果のポイント
・良質な抗体産生細胞が誕生する場である胚中心 で、B細胞 が増殖・分化する仕組みは理解されていない
・転写因子 Foxo1 が、胚中心B細胞の適切な増殖・分化に必須の機能を担っていることを解明
・今回の成果を応用し、良質の抗体 の産生を導くワクチン療法の開発に期待
概要
大阪大学免疫学フロンティア研究センターの井上毅特任助教(常勤)、新中須亮特任助教(常勤)、伊勢渉特任准教授(常勤)、黒崎知博特任教授(常勤、理化学研究所統合生命医科学研究センターグループディレクター)らの研究グループは、免疫組織に存在する、良質な抗体を産生する重要な場、「胚中心」のB細胞の働きを制御する仕組みを明らかにしました。この胚中心B細胞が適切に増殖・分化するために、転写因子であるFoxo1が必須の機能を担っていることを解明しました。
本研究成果は、米国の科学雑誌『Journal of Experimental Medicine』(3月28日(火)付け:日本時間3月28日(火)23時)にオンライン掲載されました。
研究の背景
インフルエンザウイルス感染により年間約1万人(国内)もの死者が出ているように、ウイルス・細菌感染に対する生体防御メカニズムの解明は依然として重要な課題です。われわれの体内では、ウイルス・細菌などに感染すると、脾臓やリンパ節といった免疫組織で「胚中心」という反応場が形成されます。この胚中心に存在するB細胞(胚中心B細胞)は、抗体遺伝子への変異導入を繰り返して自らの抗体の性能を高めていき、侵入した細菌、ウイルスを攻撃できる良質の抗体を作ります。しかし、この胚中心B細胞の増殖・分化を制御するメカニズムは、これまで十分に明らかにされていませんでした。
本研究の成果
同研究グループは転写因子Foxo1に着目し、B細胞から特異的に誘導的にFoxo1を欠損させることができるマウスモデルを作製し、胚中心B細胞におけるFoxo1の役割を解析しました。まず、抗原刺激を与える前のナイーブB細胞でFoxo1を欠損させ、免疫応答反応を誘導したところ、Foxo1欠損B細胞は対称細胞群と比較してより活発な増殖を引き起こしました (図1) 。一般的にFoxo転写因子ファミリーは細胞の静止状態(quiescence)をつかさどる因子と考えられており、がん細胞においてもしばしばFoxo1の機能喪失が見られることからFoxo1はがん抑制遺伝子としても知られています。このことから、Foxo1欠損に伴って増殖が活発化することはこれまでの知見から予想されるものでした。
次に胚中心形成後のB細胞において誘導的にFoxo1を欠損させたところ、意外なことに著明な胚中心B細胞の退縮、増殖の減少が見られ、Foxo1は胚中心の維持・増殖に必要であることが分かりました (図2) 。すなわち、Foxo1が胚中心ではナイーブB細胞やほかの細胞系列と逆の働きをしていることを示唆しています。
胚中心は、組織学的にdark zone(暗領域)とlight zone(明領域)に分けられます。dark zoneではB細胞が活発に増殖しながら抗体遺伝子に体細胞突然変異を導入する一方、light zoneでは胚中心B細胞が近縁に存在する濾胞樹状細胞や濾胞性ヘルパーT細胞との相互作用を通して親和性選択を受け、抗体産生細胞や記憶B細胞に分化していくと考えられています。
これまで胚中心B細胞がdark zone/light zone間をどのようなメカニズムで遷移しているかはほとんど分かっていませんでした。今回、Foxo1欠損マウスの胚中心ではこのdark zoneが選択的に失われていたことから、胚中心B細胞がlight zoneからdark zoneへ移行するためにはFoxo1が必須であることが分かりました (図3) 。
また、この移行の過程では、light zone B細胞はヘルパーT細胞への抗原提示を行い、それに応じたヘルパーT細胞からの刺激を受けとることが必要であると考えられていますが、Foxo1欠損胚中心B細胞はT細胞への抗原提示能に異常をきたしており、これがdark zoneへと移行できない原因の一つであると考えられます (図4) 。
図1 Foxo1欠損マウスの解析(胚中心形成以前)
Foxo1誘導的欠損マウスを用いて抗原刺激前にFoxo1を欠損させ、免疫4日後の脾臓における細胞数を野生型と比較。その結果、Foxo1欠損細胞は野生型の2倍以上の細胞が存在していたことから、胚中心形成以前のB細胞においては、Foxo1は細胞の増殖を負に制御していることが分かった。
図2 Foxo1欠損マウスの解析(胚中心形成後)
図1と同様にFoxo1誘導的欠損マウスを用いて、抗原刺激に伴う胚中心形成後にFoxo1を欠損させ、脾臓における胚中心を解析(左:脾臓細胞のフローサイトメトリー解析、右:胚中心B細胞数のグラフ)。その結果、図1とは反対にFoxo1欠損マウスでは胚中心B細胞の数が著しく減少することが分かった。
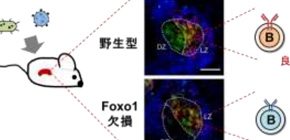
図3 Foxo1欠損マウスの脾臓切片の顕微鏡観察
胚中心形成後に誘導的にFoxo1を欠損させたのち、脾臓切片の胚中心に顕微鏡観察。濾胞B細胞(青)のない領域が胚中心を示しており(点線)、その中でも濾胞樹状細胞(赤)が存在する領域がlight zone(LZ)、存在しない領域がdark zone(DZ)を表した。野生型胚中心B細胞(緑)は、dark zone(DZ)とlight zone(LZ)両方に分布しているのに対し(左)、Foxo1欠損胚中心B細胞はlight zoneにしか存在していないことが分かった(右)。なお、濾胞(ほろう)とは多数の細胞からなる完全に閉じた袋状の構造物
図4 本研究で明らかになった胚中心B細胞におけるFoxo1の役割
Foxo1は胚中心B細胞の増殖のために重要な転写因子であり、Foxo1がないと胚中心のdark zoneが失われ、胚中心が退縮していく。また、light zoneにおいても、Foxo1は濾胞性ヘルパーT細胞への抗原提示や、T細胞からの刺激に応じたdark zoneプログラムに必要な遺伝子群の発現といった胚中心B細胞のさまざまな局面で大事な働きをしていることが分かった。Foxo1の機能をうまく制御できれば、より良い抗体産生を導くことができるようになると期待される。
さらに研究グループは、Foxo1欠損細胞の異常の原因を探るべく、網羅的遺伝子発現解析を行い、Foxo1欠損胚中心B細胞において別の転写因子Batfの発現が著しく減少していることに着目しました。Batfは胚中心B細胞のlight zoneで高い発現を示す転写因子であることが知られており、light zone B細胞において、T細胞からの刺激に応じて発現が誘導されることが分かったためです。そこでBatfをFoxo1と同じように胚中心B細胞で誘導的に欠損させるマウスを作製、解析したところ、Foxo1欠損のときと同様に胚中心が著しく退縮していくことが観察されました。さらに、Foxo1欠損胚中心B細胞にBatfを外来的に発現誘導すると、退縮していた胚中心が回復しました。このことから、Foxo1はBatfの発現誘導を介して胚中心B細胞の増殖・維持を制御していることが示唆されました。
本研究成果が社会に与える影響(本研究成果の意義)
ワクチン療法の目的は、細菌・ウイルス感染に一番有効な抗体産生を誘導することですが、本研究は、新規ワクチン開発に重要な貢献をすると考えられます。今回研究グループはマウスモデルを用いた研究から、転写因子Foxo1が、胚中心B細胞が適切に増殖・分化するために必須の機能を担っているほか、胚中心のさまざまな局面で重要な役割を果たしていることを明らかにしました。
今回の成果を応用し、Foxo1を標的として胚中心B細胞の機能を制御できれば、有効なワクチン戦略の開発につながります。
特記事項
本研究成果は、米国の科学雑誌『Journal of Experimental Medicine』(3月28日(火)付け:日本時間3月28日(火)23時)にオンライン掲載されました。
【論文タイトル】The transcription factor Foxo1 controls germinal center B cell proliferation in response to T cell help.
【著者】Takeshi Inoue, Ryo Shinnakasu, Wataru Ise, Chie Kawai, Takeshi Egawa, Tomohiro Kurosaki
本研究は、大阪大学、理化学研究所が共同で行ったものです。
大阪大学免疫学フロンティア研究センター(IFReC)は、日本が科学技術の力で世界をリードするため「目に見える世界的研究拠点」の形成を目指す文部科学省の世界トップレベル研究拠点プログラム(WPI)に採択されています。
参考URL
免疫学フロンティア研究センター分化制御研究室-IFReC-
http://lymph.ifrec.osaka-u.ac.jp/index_j.html
用語説明
- 抗体
B細胞が産生するタンパク質で、特定のタンパク質など抗原を認識して結合し無毒化する働きを持つ。例えば、インフルエンザにはインフルエンザ専門のB細胞とそれが作り出す抗体がある。
- 胚中心
免疫応答の際にリンパ節や脾臓などの免疫組織において誘導される微小構造。ここではB細胞が活発に増殖するとともに、抗体遺伝子に変異を入れてより良い抗体を産生できるようになる。胚中心は構造学的にdark zone(暗領域)とlight zone(明領域)に分けられる。
- B細胞
免疫細胞の一種で、細胞表面にあるB細胞抗原受容体と呼ばれるタンパク質で病原体などの抗原を認識し抗体を産生する。B細胞は、抗原の刺激に応じて胚中心B細胞、抗体産生細胞および記憶B細胞へと分化する。
- 転写因子
DNA上に存在する転写を制御する領域に結合し、特定の遺伝子の働きを促進、あるいは抑制する機能を持つタンパク質群。
- Foxo1
フォークヘッド型転写因子Forkhead box-containing protein,O1略。さまざまな組織、細胞で働いているが、胚中心B細胞における機能は不明であった。
