世界初!大麻が脳に悪影響を与えることを科学的に証明
大麻の有効成分:カンナビノイドが神経回路を破綻
本研究成果のポイント
・長年不明であった大脳皮質内の神経回路形成の重要なメカニズムを解明
・大麻(マリファナ)の有効成分でもあるカンナビノイド が、大脳皮質神経回路の破綻をきたすことを発見
・大麻や危険ドラッグが脳に悪影響を与えることの科学的根拠を明らかにしたとともに、脳損傷、認知症での機能回復に応用できる可能性も期待できる成果
リリース概要
大阪大学大学院医学系研究科解剖学講座(分子神経科学)の木村文隆准教授を中心とする研究グループは、大脳皮質の神経回路形成に複数のメカニズムが関与することを解明しました。同時に、大麻の有効成分でもあるカンナビノイドと類似した物質が回路形成に重要な働きをしており、不要な配線(シナプス)を刈り込むこと、つまり、外来性に大麻を摂取すると、必要な配線まで刈り込まれ、神経回路の破綻をきたすことを世界で初めて明らかにしました (図1) 。
これまで、神経回路ができるのには神経活動が重要な役割をすることはわかっていましたが、どのような神経活動が回路形成に関わっているのかは長い間不明でした。また、大脳皮質の一部では、シナプス 前後の同期した活動によってシナプスができていくメカニズムがあることは知られていましたが、特に視床 から大脳皮質への投射の形成では一旦広範に投射した後に、余計な配線が整理されて限局した投射に収束していくのに、どのような神経活動が関わっているのか不明でした。今回、不要な配線ではシナプス前後の同期した活動により、カンナビノイド類似物質が放出され、これが余計な配線を整理していることがわかりました。
本成果は、大麻や危険ドラッグが脳に悪影響を与えることの科学的根拠を明らかにしたものです。カンナビノイドの機能を止めることによって、神経回路の破綻を抑制できる可能性もあり、今後、脳損傷、認知症での機能回復に応用できる可能性も期待されます。
本研究成果は、米国科学誌「Journal of Neuroscience」に、6月30日(木)午前6時(日本時間)に公開されました。
図1
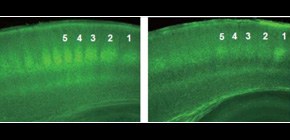
左:正常な大脳皮質への視床投射。視床線維だけが蛍光を発するマウスからの写真。中間層に視床からの投射の密集が観察できる(1~5の下)。 右:マリファナの有効成分であるΔ 9 THC(Δ9テトラハイドロカンナビノール。カンナビノイドの1つ)を投与されたマウスからの写真。視床からの投射が劇的に退縮していることが観察できる(1~5の下)。
研究の背景
これまで、神経回路の形成や精緻化にはシナプス前後の神経の活動が大きな影響を及ぼすことが知られていましたが、具体的にシナプス前後のどのような活動がどのようにして形態的変化をもたらすのかはわかっていませんでした。特に、視床から大脳皮質への投射の形成(視床―皮質投射)ではより複雑で、未熟な大脳皮質に一旦広く投射ができた後、大脳皮質の成長に伴って、不要な投射が削られ、正しい投射先だけが残っていくというように2段階に進みますが、そのメカニズムは不明でした。
大脳皮質の他の部位(4層-2/3層間シナプス)では、シナプス前後の細胞の発火順序に依存してシナプスの強度がきまるルール(スパイクタイミング依存性可塑性:STDP)が働くことが知られていましたが、木村准教授らの研究グループでは、このシナプス(4層-2/3層間シナプス)でも回路ができている最中にはSTDPのルールが異なっており、成長のある段階でルールが急に変化することを見つけていました。今回、視床と大脳皮質のシナプスでも投射形成に伴って同様にSTDPの変化がある可能性に着目し、検討を行いました。
本研究成果の内容
今回、木村准教授らの研究グループは、視床―皮質投射ができる時、最初はシナプス前後(視床細胞と大脳皮質細胞)の同期した活動によってシナプスが強化され、広い範囲に投射が伸びた後一部の投射先を除いて今度は同期した活動がシナプスを弱化されるというルールに変化し、余計な投射が刈り込まれ整然とした投射ができることを見出しました (図2) 。また、このシナプス弱化時には同期した活動によって神経細胞からカンナビノイドが放出されること、さらに、放出されたカンナビノイドによって不要な神経投射が退縮することがわかりました。同時に、カンナビノイドを外来性に摂取しても神経投射が退縮することも確認されました。さらに、カンナビノイドの受け手であるカンナビノイド受容体の機能を遺伝的に欠如させると余計な投射の刈り込みがなくなり、無秩序な投射のまま残ってしまうことが判明しました。
図2
左:正常な視床皮質投射、2例。視床線維は4層の赤い矩形領域(バレル)内に収束する。 右:カンナビノイド受容体欠損動物の異常な視床皮質投射、2例。視床線維は4層のバレルを無視した投射を示す。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、神経回路形成のメカニズムの理解がさらに進むことが期待されます。また、脳損傷や認知症の治療薬につながる可能性も考えられます。さらに、大麻摂取が脳の正常な発達に障害を与えることを科学的に証明したことから、大麻や危険ドラッグの乱用減少への啓発にも貢献が期待されます。
研究者のコメント
カンナビノイドは気軽に気分が高揚し、無害だと考えられて、気軽に手を出す人が後を絶ちませんが、実は間違った配線を削っていきながら、正しい神経回路を作るのに非常に重要であり、摂取することによって、本来の正しい配線までも削られていきますので、大変危険です。特に、若い世代に影響が大きいと考えられますから、絶対に手を出すのはやめましょう。
特記事項
本研究成果は、6月30日(木)午前6時(日本時間)[6月29日(水)午後5時(米国東部時間)]に米国科学誌「Journal of Neuroscience」(オンライン版)に掲載されました。
タイトル:Developmental switch in spike timing-dependent plasticity and cannabinoid-dependent reorganization of the thalamocortical projection in the barrel cortex
著者名:Chiaki Itami, Jui-Yen Huang, Miwako Yamasaki, Masahiko Watanabe,Hui-Chen Lu,Fumitaka Kimura
なお、本研究は、埼玉医科大学医学部生理学教室伊丹千晶講師、Baylor College of Medicine, Indiana UniversityのJui-Yen Huang博士、Hui-Chen Lu教授、北海道大学解剖学教室山崎美和子講師、渡辺雅彦教授の協力を得て行われました。
参考URL
大阪大学大学院医学系研究科解剖学講座(分子神経科学)HP
http://www.med.osaka-u.ac.jp/pub/molneu/index.html
用語説明
- カンナビノイド
大麻(マリファナ)に含まれ、摂取による精神作用を起こす有効成分(Δ THC)と同様の作用を起こす化学物質類の総称。神経細胞に直接作用し、神経細胞間(シナプス ※2 参照)での情報伝達を阻害する。その受容体は脳内に広く存在し、G蛋白と協力して作用する受容体類(G蛋白共役型受容体)の中では脳内で最も多く存在するものの一つ。
- シナプス
神経細胞間のつなぎ目で、ここでは情報が一方向(シナプス前細胞からシナプス後細胞へ)に受け渡される。この時の反応の大きさが、シナプス同士の結合の強さを決め、情報処理を大きく左右する。
- 視床
間脳の一部。大脳皮質への入力の入り口。
