遺伝性パーキンソン病の核酸医薬を用いた新規治療法に新展開!
原因蛋白質の蓄積を抑制し、病気の発症・進行を抑制する治療法開発に光
本研究成果のポイント
・遺伝性パーキンソン病(PARK4)の原因である、蛋白質のシヌクレイン の蓄積抑制に動物モデルで成功
・これまで病気の発症・進行を抑制する根本的な治療法は存在せず、治療法開発に新展開をもたらす成果
・遺伝性のパーキンソン病だけでなく、大多数を占める孤発性のパーキンソン病や認知症(レヴィー小体型)の治療への応用にも期待
概要
遺伝性パーキンソン病(PARK4)は蛋白質のシヌクレインが蓄積・凝集することによって、神経細胞死が引き起こされ発症します。大阪大学大学院医学系研究科神経内科学の望月秀樹教授、中森雅之助教、上原拓也医員らは、同大学院薬学研究科創薬センター・小比賀聡教授、東京医科歯科大学脳神経病態学・横田隆徳教授らと共同研究で、新規修飾核酸AmNA を搭載したGapmer型核酸医薬 が、シヌクレインの蓄積を抑制し、遺伝性パーキンソン病の症状を改善することを動物モデルで証明しました。
これまで遺伝性パーキンソン病の発症や進行を遅らせる根本的治療法は存在せず、本研究グループの研究成果および研究手法が画期的な治療法になるものと期待されます。
なお、本研究成果は平成28年5月20日(金)開催の、第57回日本神経学会学術大会にて中森雅之助教が発表しました。
研究の背景
パーキンソン病はアルツハイマー病についで二番目に多い進行性の神経変性疾患です。症状を改善する治療薬は存在しますが、進行を抑制する根本的な治療法は存在しません。そのため、寝たきりになる患者も存在し、大きな社会問題になっており、全世界で進行を抑制する治療法開発が進められています。将来的には、本治療法が遺伝性パーキンソン病(PARK4)だけでなく、大多数を占める孤発性パーキンソン病の治療にも適応になることが期待されます。
今回の成果
遺伝性パーキンソン病であるPARK4は、シヌクレイン遺伝子の重複により過剰なシヌクレインが蓄積することが原因です。本研究では、過剰なシヌクレインを核酸医薬で抑制する戦略で治療開発を進めました。抑制効果を高めるため、AmNAという高い酵素耐性能を持つ特殊な修飾核酸を用い、さらには目的のタンパク質をコードするために必要な配列最適化プログラムなどを用いて、シヌクレイン抑制効果の最も高い配列で遺伝子抑制効果を発揮するGapmer構造を決定しました。その上で、パーキンソン病モデルマウスの脳室内へAmNA搭載Gapmer型核酸医薬を投与することにより、脳細胞でシヌクレインの蓄積を抑制することに成功しました (図) 。特に臨床での投与法に近い脳室内投与で、核酸医薬が十分に脳細胞へ浸透し、標的抑制効果を示した点で、今後の臨床応用が期待されます。
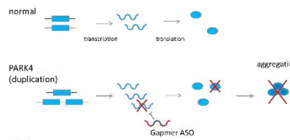
図
Gapmer型核酸医薬(ASO)が、遺伝性パーキンソン病PARK4において過剰に生成されたシヌクレインを分解することにより、シヌクレインの蓄積を防ぐ。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果は遺伝性パーキンソン病(PARK4)の有効な治療法として大変期待されるだけでなく、孤発性パーキンソン病やレヴィー小体型認知症も異常シヌクレインの蓄積によって生じることが知られているため、本研究成果のこれら疾患への応用も期待されます。
特記事項
本研究成果は平成28年5月20日(金)開催の第57回日本神経学会学術大会にて発表されました。
【発表学会】第57回日本神経学会学術大会 ホットトピックス15「Gene therapy and regeneratative medicine」
【発表演題名】Gene therapy with antisense oligonucleotides for neurological and neuromuscular disorders
【演者】Masayuki Nakamori, Hideki Mochizuki
本研究は、日本医療研究開発機構平成27,28年度橋渡し研究加速ネットワークプログラム(シーズB)の支援対象課題です。 http://www.amed.go.jp/news/program/050120151225_kettei_besshi01.html
参考URL
大阪大学大学院 医学系研究科 神経内科学
http://www.med.osaka-u.ac.jp/pub/neurol/myweb6/Top.html
用語説明
- 遺伝性パーキンソン病
遺伝性パーキンソン病(PRAK4):
振戦(ふるえ)、動作緩慢、筋強剛(筋固縮)、姿勢保持障害(転びやすいこと)を主な運動症状とする進行性の神経変性疾患であるパーキンソン病のうち、シヌクレイン遺伝子の重複により発症する遺伝性のもの。過剰に産生されたシヌクレインが蓄積・凝集することが原因とされている。また認知症状の合併も多いとされている。
- シヌクレイン
シヌクレイン(αシヌクレイン):
神経細胞内に存在する蛋白質で、機能は不明である。シヌクレインが蓄積し、凝集することで神経細胞障害を来す。こうした凝集体は、パーキンソン病のみならずレヴィー小体型認知症でもみられ、幅広い神経疾患を引きおこすとされている。
- 新規修飾核酸AmNA
架橋型修飾核酸のひとつで、高い標的結合性、DNA分解酵素耐性を持ち、また肝臓への毒性が低い。
- Gapmer型核酸医薬
両側に数塩基の修飾核酸、中央部に5-10塩基程度の非修飾DNAで構成される核酸医薬。特定の遺伝子発現を制御する標的mRNAと結合すると、RNA分解酵素を活性化し、標的を切断し、特定の疾患の発症を抑制する作用をもつ。こうした形状をもつ核酸医薬は、ハンチントン病や筋強直性ジストロフィーなど、ほかの神経筋疾患への治療応用が進んでいる。
