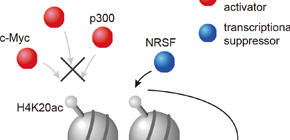
世界初!全く新しい種類の細胞核の目印を発見
代謝や循環器などの疾患等の発症・進展のメカニズムの解明に期待
本研究成果のポイント
・植物細胞にのみ存在するとされてきた細胞核の蛋白質:ヒストン修飾H4K20ac が哺乳類細胞に存在することを証明
・遺伝子発現増強に関与するとされてきたアセチル化ヒストン修飾 内に、遺伝子発現抑制に関わる構造を発見
・代謝疾患、循環器疾患、腎疾患、癌などの様々な疾患の発症、進展のメカニズムの解明に期待
概要
大阪大学大学院医学系研究科内科学講座(腎臓内科学) 猪阪善隆 教授、同先端移植基盤医療学寄附講座 高原史郎 寄附講座教授、貝森淳哉 寄附講座准教授、同蛋白質研究所 高尾敏文 教授、東京工業大学大学院生命理工学研究科 木村宏 教授、九州大学生体防御医学研究所 大川恭之 教授らの研究グループは、これまで動物細胞では間接的にしか存在が示されていなかった細胞核の目印である蛋白質:ヒストン修飾H4K20acの存在を、質量分析を用いて証明しました。また、H4K20acに対する抗体を作成し、クロマチン免疫沈降法 と次世代シークエンサー 、スーパーコンピューターを用いた解析で、今まで知られていたアセチル化は、発現頻度の高い遺伝子のプロモーター部位 に集積するのに対して、H4K20acは発現頻度の低い遺伝子のプロモーター部位に集積することを見出し、H4K20acが、全く新しい種類のヒストン修飾であることを発見しました。
近年、様々な病気の発症・進展に遺伝子配列以外の遺伝子発現の制御・伝達システムであるエピジェネティック な因子が深く関与することが知られるようになってきました。遺伝子DNAが巻きついているクロマチンの構成要素であるヒストンには、エピジェネティックな因子として、蛋白質自身の働きを変化させる様々な翻訳後修飾 がなされることが知られており、この修飾の種類が遺伝子発現に影響を与えることがわかっています。
本研究で発見された全く新しい種類のヒストン修飾H4K20acを用いて、糖尿病をはじめとする代謝疾患、心肥大をはじめとする循環器疾患、腎疾患、癌などの様々な疾患の発症・進展のメカニズムの解明が期待されます。
本研究成果は、英国時間4月11日(月)午前10時に英国科学雑誌「Scientific Reports」オンライン版で公開されました。
研究の背景
生物の細胞は、遺伝子の発現の必要なときにスイッチオンしたり、スイッチオフしたりして環境の変化に適応しています。これまで遺伝子発現に影響を与えるエピジェネティックな因子であるヒストン修飾は、大きく分けて遺伝子の発現のスイッチオンに関わるものと、スイッチオフに関わるものに分けられていました。特にアセチル化ヒストン修飾は陰性に荷電していることから、同じく陰性に荷電したDNAとは互いに反発して、転写因子が入り込むスペースができて、遺伝子の発現をスイッチオンに関わっていることは、遺伝学の常識でした (図1) 。また、H4K20acは、植物細胞でのみ存在することがわかっていましたが、哺乳類細胞では存在が間接的にしか示されていませんでした。
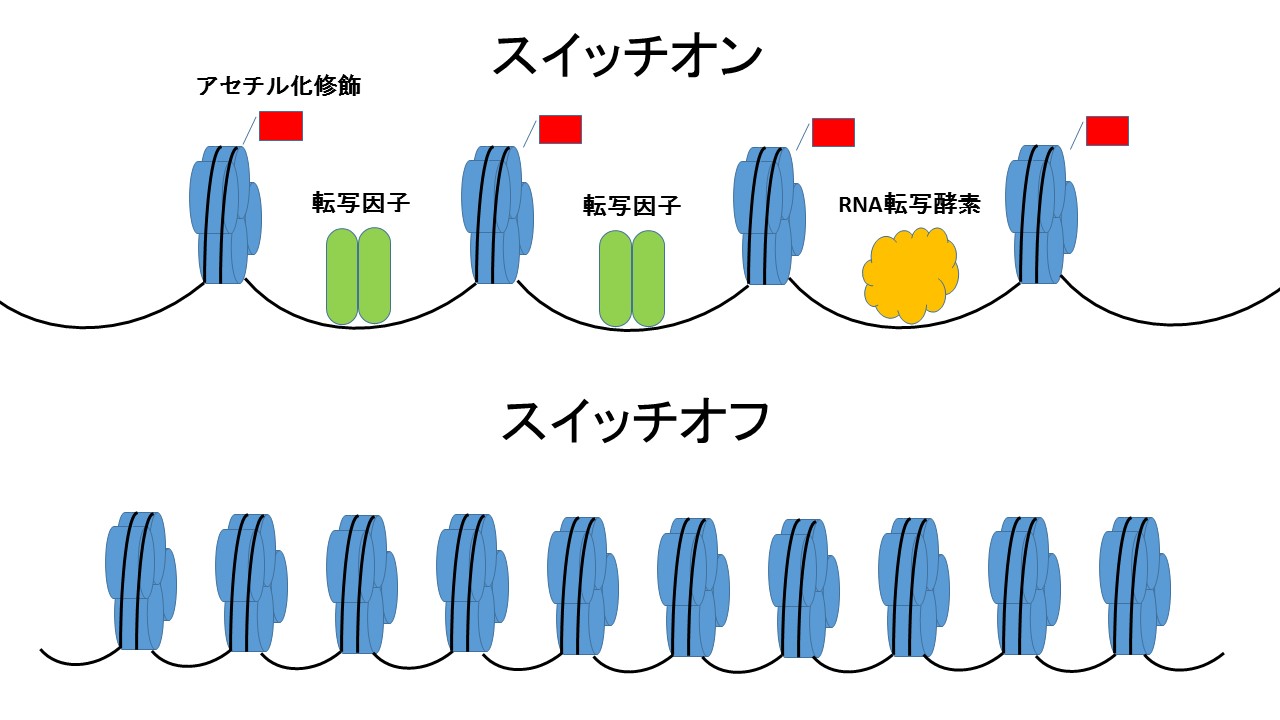
図1
従来、アセチル化ヒストン修飾は遺伝子のスイッチオンのみに関係すると考えられてきた。
研究の成果
研究グループの貝森淳哉寄附講座准教授は、哺乳類細胞から大量のヒストン蛋白を抽出し、大阪大学蛋白質研究所高尾研究室の質量分析機を用いて、精密に分子量を測定することによりH4K20acが、哺乳類細胞に存在することを証明しました (図2) 。また、このヒストン修飾に対する抗体を作成し、貝森寄附講座准教授がクロマチン免疫沈降したサンプルを九州大学大川研究室で次世代シークエンサーを用いて解析し、このデータを九州大学前原一満研究員がスーパーコンピューターを用いて解析し、世界中のデータベースに存在する既知のヒストン修飾のデータと網羅的に比較することによって、H4K20acが発現量の低い遺伝子のプロモーターに集積していること、H4K20acの集積しているプロモーター部位には、遺伝子発現増強因子は近づけないが、遺伝子発現抑制因子が近づくことができることを発見しました (図3) 。

図2
H4K20acの存在を、分子量を正確に測定することにより証明した。
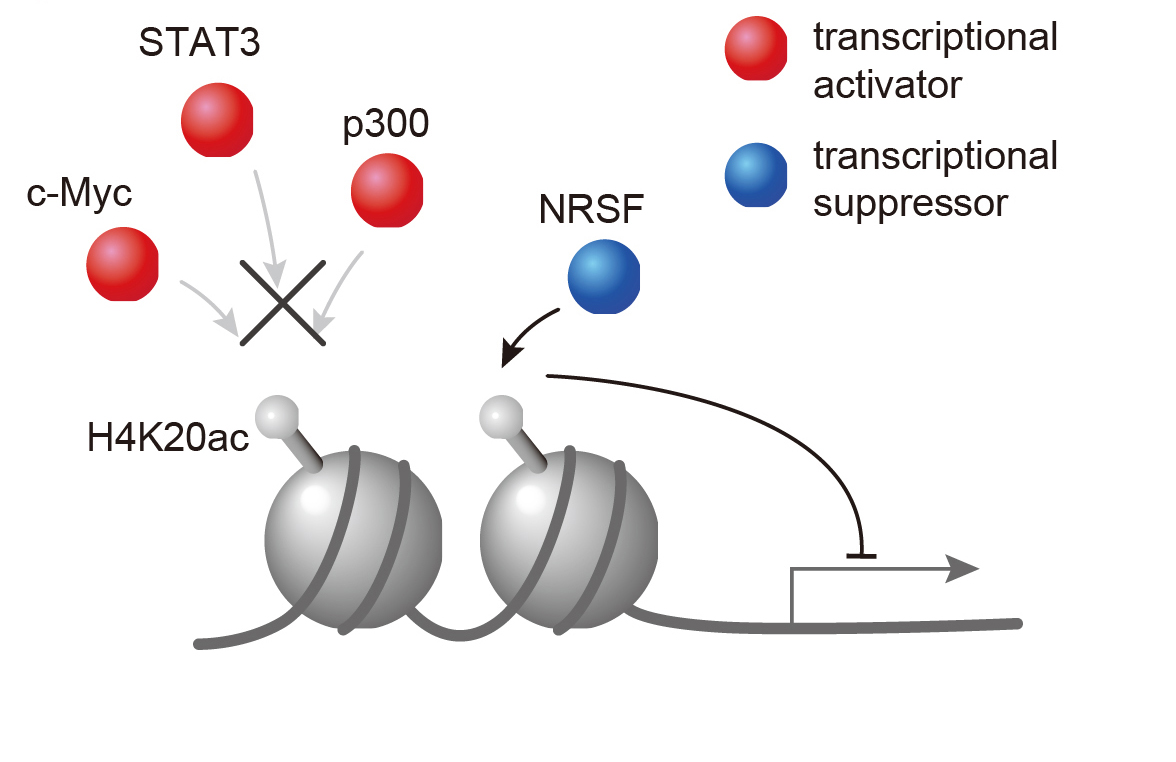
図3
ヒストン修飾H4K20acが、発現していない遺伝子のプロモーター部位に存在することを説明。遺伝子発現増強因子(transcriptional activator)は、H4K20acに近づくことができないが、遺伝子発現抑制因子(transcriptional suppressor)は近づくことが出来る。
本研究成果が社会に与える影響(本研究成果の意義)
ヒストン修飾をはじめとするエピジェネティックな因子は、様々な疾患の発症・進展に関係することが、疫学研究から明らかになっており、そのメカニズムに興味が集まっています。本研究成果で発見された全く新しい種類のヒストンアセチル化修飾H4K20acを用いて、糖尿病をはじめとする代謝疾患、心肥大をはじめとする循環器疾患、腎疾患、癌などの様々な疾患の発症・進展のメカニズムついての研究が進むことが期待されます。
特記事項
本研究成果は、英国科学雑誌「Scientific Reports(サイエンティフィック リポーツ)」オンライン版に4月11日(月)午前10時(英国時間)に掲載されました。
論文タイトル:Histone H4 lysine 20 acetylation is associated with gene repression in human cells.
著者:Jun-Ya Kaimori, Kazumitsu Maehara, Yoko Hayashi-Takanaka, Akihito Harada, Masafumi Fukuda, Satoko Yamamoto, Naotsugu Ichimaru, Takashi Umehara, Shigeyuki Yokoyama, Ryo Matsuda, Tsuyoshi Ikura, Koji Nagao, Chikashi Obuse, Naohito Nozaki, Shiro Takahara, Toshifumi Takao, Yasuyuki Ohkawa, Hiroshi Kimura, and Yoshitaka Isaka
参考URL
大阪大学大学院医学系研究科先端移植基盤医療学HP
http://www.att.med.osaka-u.ac.jp/
用語説明
- ヒストン修飾H4K20ac
長いゲノムDNAが小さな核の空間に収納されるために、ヒストンの周りに巻きついてクロマチンと言われる構造を作ります。DNAが巻きつくヒストンは、コアヒストンH2A、H2B、H3、H4が2個づつ集まって8量体の構造を作っています。このH4ヒストン分子の20番目のリジン残基にアセチル基がついた修飾が、ヒストン修飾H4K20acになります。
- アセチル化ヒストン修飾
アセチル化とは、蛋白質にアセチル基の修飾がなされることをいいます。ヒストン修飾の中で、アセチル化は遺伝子発現のスイッチオンに関わっていると言われています。それは、アセチル化自体が陰性に帯電しているため、同じく陰性に荷電しているDNAと反発して空間が出来き、その空間に転写因子が入って行き易くなるためと考えられています。
- クロマチン免疫沈降法
クロマチン構成蛋白、蛋白修飾及び遺伝子結合蛋白に対する抗体による免疫沈降反応。この抗体に対する蛋白及び蛋白修飾が存在する部位の遺伝子配列を明らかにするために行われます。
- 次世代シークエンサー
シークエンサーは、DNA配列を正確に読み取ることができる機械です。従来のキャピラリーシークエンサーが数百bpのDNA配列を読み取れるのに対して、次世代シークエンサーは最高で100Gbp(10 11 bp)のDNA配列を読み取ることが可能です。
- プロモーター部位
遺伝子の上流に位置し、遺伝子の発現を調節する部位のことをいいます。
- エピジェネティック
エピジェネティック(epigenetic):
遺伝子DNAの配列以外の因子により、細胞分裂後も継承される遺伝子発現あるいは細胞表現型の変化を研究する分野。実際には、DNAのメチル化やヒストン修飾がエピジェネティックな因子とされる。近年、様々な病気の発症、進展にエピジェネティックな因子が深く関与することが知られるようになって、広く注目を集めている。
- 翻訳後修飾
蛋白質は、遺伝子からアミノ酸配列に翻訳された後、様々に化学的な修飾がなされることが知られています。例えば、リン酸化、アセチル化、メチル化などがこれにあたります。これらの修飾を受けることで、蛋白質自身の働きが変化します。
