間違いだらけの修復が、がんを引き起こす!?
放射線等によるDNA損傷修復の分子メカニズムを解明
本研究成果のポイント
・DNA損傷応答システムが十分に機能しないと、傷ついたDNAの修復時に除去されるべきタンパク質が残り、誤った方法で修復されることで細胞ががん化してしまうことを発見
・DNAの修復がどのような不具合・過程を経て細胞ががん化するのか、放射線の影響などの詳細は不明だった
・放射線によるDNAの傷により細胞ががん化する初期の分子メカニズムや、放射線被曝によって引き起こされる発がんの分子メカニズムの解明に期待
リリース概要
細胞のがん化は、何がきっかけで始まるのでしょうか。
大阪大学蛋白質研究所の篠原美紀准教授の研究グループは、遺伝情報であるDNAが放射線で傷ついたときに活性化する本来の細胞機能であるDNA損傷応答システムが十分に機能しないと、DNAの傷は修復されるものの、元通りの情報にはならず間違いを残したまま傷だけを修復してしまうことを発見しました。
細胞ががん化する原因のひとつとして、物理的に遺伝情報源が壊れてしまうことが考えられています。しかし、私たちの体には壊れる前に治す仕組み(DNA修復機構)があるため、その仕組みがどのような不具合・過程を経て、正常な細胞ががん細胞へと変貌を遂げてしまうのか、なぜ放射線はがんを引き起こしてしまうのか、詳細はあまりわかっていません。
本研究グループでは、より正確に修復するためにDNAの傷が加工される途中で、本来そこで働くべきではない、傷から除外されるべきKuタンパク質 が除去されずに活性を持った状態で残っていることで、加工途中のDNAを誤った方法で修復してしまっていることを、パン酵母の二種類の変異株(Xrs2 とTel1 )を用いて明らかにしました。ヒトで同じ働きをするこれらの遺伝子が変異すると、どちらの場合も、高発がん性と免疫不全を示す遺伝病になることが知られています。また、遺伝子変異がないヒト由来のがん細胞でもこれらの遺伝子に変異が見つかることが知られています。
この研究は、ヒト細胞がどのようにがん細胞へと変貌を遂げるのか、特に放射線によるDNAの傷によって、細胞ががん化する初期の分子メカニズムを、原始的な真核生物であるパン酵母をモデルとして明らかに出来る可能性があることを示しています。また、今後ヒト細胞での検証を行うことで、放射線被曝によって引き起こされる発がんの分子メカニズムを明らかに出来る可能性があります。
本研究成果は、米国科学誌「PLoS Genetics」に3月19日(土)午前3時(日本時間)に掲載されました。
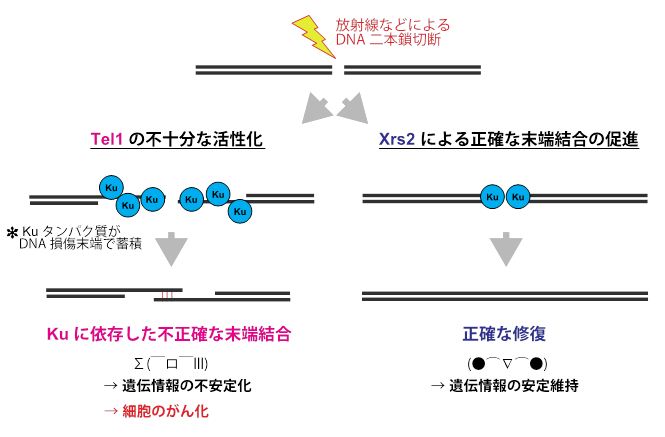
ゲノムDNAに放射線等によりDNA二本鎖切断が入ると通常は速やかにかつ正確に修復される(右)。一方、Tel1の機能が不十分な状態で、末端結合が速やかに行われないとKuタンパク質が単鎖化されたDNA上に蓄積して遺伝情報に間違いが残るような修復をしてしまう(左)。
研究の背景
【がんは細胞のDNA遺伝情報が壊れてしまうことで起こる病気である】
約60兆個の細胞から構成される私たちの体は、ひとつの受精卵から分裂することで作られます。そのため、体中のどの細胞も同じ遺伝情報をもとに活動しています。ただし、体の部分によってどの遺伝情報を使うのかが決まっていて、その制御(ルール)も遺伝情報をもとにしています。大事な遺伝情報が壊れている、ルールが書き換えられる、あるいは間違って伝えられるなどの理由で本来の機能を失って、増殖することだけを細胞が始めてしまうとがん細胞になってしまいます。
細胞ががん化する原因には様々ありますが、そのひとつとして物理的に遺伝情報源が壊れてしまうことが考えられています。放射線や特定の化学物質をはじめ、私たちが生きていくために欠かせない太陽光や酸素までが遺伝情報を壊す原因となることが知られています。しかし、私たちの体には壊れる前に治す仕組み(DNA修復機構)があり、その仕組みが外敵から遺伝情報を守ってくれています。その仕組みがどのような不具合を起こすとどのような過程を経て、正常な細胞ががん細胞へと変貌を遂げてしまうのか?なぜ、放射線はがんを引き起こしてしまうのか?詳細はあまりわかっていません。
研究の成果
【がんの原因は、DNA損傷修復時に不要な道具を現場に残してしまい、間違いを多く残したまま修復を終えてしまうことにあった!?】
放射線は生物の設計図であるゲノムDNAを傷つけてしまいます。しかし、通常私たちの細胞はその傷を元通りに治す機能、DNA損傷修復機能を持っています。DNA損傷修復機能は多くの生物の間で非常に保存された機能として知られており、進化上とても離れているパン酵母とヒトの間でも同様の機能を持つタンパク質が多く働いています。その中の酵母Xrs2(ヒトではNbs1)と酵母Tel1(ヒトではATM)のDNA損傷修復機能に注目して解析を行いました。
ヒトNbs1タンパク質のある機能部位が働かなくなる変異が入ると、高発がん性を特徴とする遺伝病になることが知られています。酵母のXRS2遺伝子にヒト遺伝病型の変異(xrs2変異株)を入れると、傷ついたDNAは治されますが、傷口のDNA配列が変異のない酵母と比較して多くの間違いを伴って修復されることを見つけました。そして、その原因としてxrs2変異株ではDNA損傷応答に重要なTel1タンパク質の機能が十分に発揮されないことにあることを突き止めました。
本来、DNAを修復する場合、断裂した末端を即座に繋いでしまう非相同末端結合(NHEJ)と、時間はかかるがより正確な相同組換えという2つの選択肢があり、細胞は何らかの基準でどちらの方法を採用するかを決定しています。実は、DNA損傷が相同組換えで修復される過程では、DNA損傷近傍のDNA二本鎖を消化して、1本鎖にする必要があります。tel1変異株あるいはxrs2変異株では、相同組換えを行うために1本鎖に加工した傷の部分に、本来不要であることから外されているはずのKuタンパク質が、ずっとDNAの傷についたままになっていることを明らかにしました。Kuタンパク質はNHEJで断裂した末端同士をつなぎ止める働きをするタンパク質です。つまり、違う方法で治すための道具である、Kuタンパク質が本来働くべきでないところでDNA末端を無理矢理結合させてしまい、結果として修復はできるもののDNA情報が間違いだらけになってしまうと考えられます。細胞のがん化はゲノムDNAの情報が壊れてしまう、あるいは間違いが固定化することで起ります。ヒトの細胞内でもNbs1やATMが同様に機能することで、DNA損傷修復の正確性を守ることでがん細胞になることを防いでいる可能性があります。
本研究成果が社会に与える影響(本研究成果の意義)
細胞のがん化は、何がきっかけで始まるのか?今回は放射線などによって引き起こされるタイプのDNA損傷(DNA二本鎖切断)をパン酵母を用いて解明したことから、今後、ヒト細胞での検証を行うことによって、今後放射線被曝によって引き起こされる発がんの分子メカニズムを明らかに出来る可能性があります。特に今回、不要なKuタンパク質のDNA損傷部位からの「適切な除去」がカギを握るステップであることを明らかにしたことから、今後、その制御メカニズムを理解することで防御の可能性についても検討できるようになると期待されます。
特記事項
本研究成果は、米国科学誌「PLoS Genetics」に3月19日(土)午前3時(日本時間)に掲載されました。
【論文タイトル】The MRX Complex Ensures NHEJ Fidelity through Multiple Pathways Including Xrs2-FHA–dependent Tel1 Activation
【著者】Daichi Iwasaki 1, 2 , Kayoko Hayashihara 1 , Hiroki Shima 3, † , Mika Higashide 1, 2 , Masahiro Terasawa 1 , Susan M. Gasser 4 and Miki Shinohara
参考URL
論文掲載先(PLoS Genetics)
http://dx.plos.org/10.1371/journal.pgen.1005942
大阪大学蛋白質研究所 プレスリリース
http://www.protein.osaka-u.ac.jp/achievement/the-mrx-complex/
大阪大学蛋白質研究所 篠原研究室HP
http://www.protein.osaka-u.ac.jp/genome/index.html
用語説明
- Kuタンパク質
Ku70/Ku80からなるタンパク質複合体で、DNA二本鎖切断の断裂末端に結合して末端が離れないように近づける機能があると考えられている。非相同末端結合による修復に必須の因子。
- Xrs2
酵母からヒトまで真核生物で広く保存されているタンパク質で、DNA二本鎖切断がおこるとその修復の初期段階でDNA損傷部位に呼び込まれて、DNA損傷応答反応に中心的な機能を果たす。それ自身では特別な活性を持つタンパク質ではなく、様々な修復に必要なタンパク質と結合してその活性を助ける役目がある。ヒトでこのタンパク質(Nbs1)が機能しないとナイミーヘン症候群という高発がん性、放射線高感受性、小頭症、免疫不全等を特徴とする遺伝病になる。
- Tel1
Xrs2によってDNA損傷部位に呼び込まれるタンパク質リン酸化酵素。DNA修復に必要なタンパク質を損傷部位で活性化する役割がある。ヒトでこのタンパク質(ATM)が機能しないと、Ataxia telangiectasiaという、神経失調、高発がん性、放射線高感受性、免疫不全等を特徴とする遺伝病になる。
