パーキンソン病の新規治療法の開発に成功
タンパク質ネクジンがミトコンドリア障害による神経細胞死を防ぐ
本研究成果のポイント
・神経細胞内に存在するタンパク質ネクジン がミトコンドリアを増やし、パーキンソン病 の進行を抑制することを動物モデルで証明
・ネクジンは老化によって生じるミトコンドリア障害 も防ぐことを発見
・パーキンソン病の画期的な治療法になりうるとともに、ミトコンドリア障害によって生じる他の神経変性疾患の予防・治療法開発にも期待
概要
ミトコンドリアが傷つくことで、パーキンソン病における神経細胞死が引き起こされます。大阪大学蛋白質研究所神経発生制御研究室の吉川和明教授、長谷川孝一助教(研究当時)、同大学院医学系研究科神経内科学の望月秀樹教授の研究グループは、神経細胞内に存在するタンパク質のネクジンがミトコンドリアの働きを促進するタンパク質PGC-1α を安定化し、ミトコンドリア障害による神経細胞死を防ぐことを発見しました。さらに、モデル動物にネクジンの遺伝子を導入することによって、神経細胞死を防ぎ、パーキンソン病の進行を抑制することにも成功しました。
パーキンソン病は、発症や進行を遅らせるという根本的な治療法はいまのところありませんが、本研究グループの研究成果および研究手法がこれらの画期的な治療法になるものと期待されます。
なお、本研究成果はNature Communicationsの電子版に3月14日(月)午前10時(英国時間)に掲載されました。
研究の背景
パーキンソン病はアルツハイマー病についで二番目に多い進行性の神経変性疾患であり、進行を抑制する根本的な治療法は存在しません。パーキンソン病の症状を改善する治療薬はあるものの、進行性のために寝たきりになる方もおり、大きな社会問題になっています。そのため、全世界で進行抑制が期待できる治療法開発が進められています。
今回の成果
PGC-1αは、ミトコンドリアの生合成と機能を促進する鍵タンパク質ですが、神経細胞内のPGC-1αを人為的に増加させることは困難でした。本研究グループは、ネクジンが神経細胞中のPGC-1αのタンパク質分解を防いで安定化することに着目し、ネクジンを使って神経細胞内のミトコンドリアを増やすことに成功しました。さらに、パーキンソン病の細胞モデルや動物モデルにネクジンの遺伝子を導入すると、パーキンソン病で障害されるドパミン神経細胞死が抑制されることを確認しました。また、ネクジンを欠損するマウスが老齢になると、パーキンソン病で侵される黒質のドパミン神経細胞が障害されやすくなるため、ネクジンがドパミン神経細胞の保護に働いている、つまり老化によって生じるミトコンドリア障害も防ぐことも証明しました。
パーキンソン病の神経細胞死の機序としてミトコンドリアが障害されることが古くから知られています。健康なドパミン神経細胞に豊富に存在するネクジンは、PGC-1αを安定化して神経変性を防ぐために重要な働きをしていたのです。
なお、今回神経細胞内にネクジンの遺伝子を正確に導入するためにアデノ随伴ウイルス(AAV)ベクター を使用しました。すでにAAVベクターを用いたパーキンソン病の遺伝子治療は、日本でも開始されており治療への道は開いています。さらに、今回の成果は、脳内でネクジンを増加させるような治療薬の開発にもつながります。
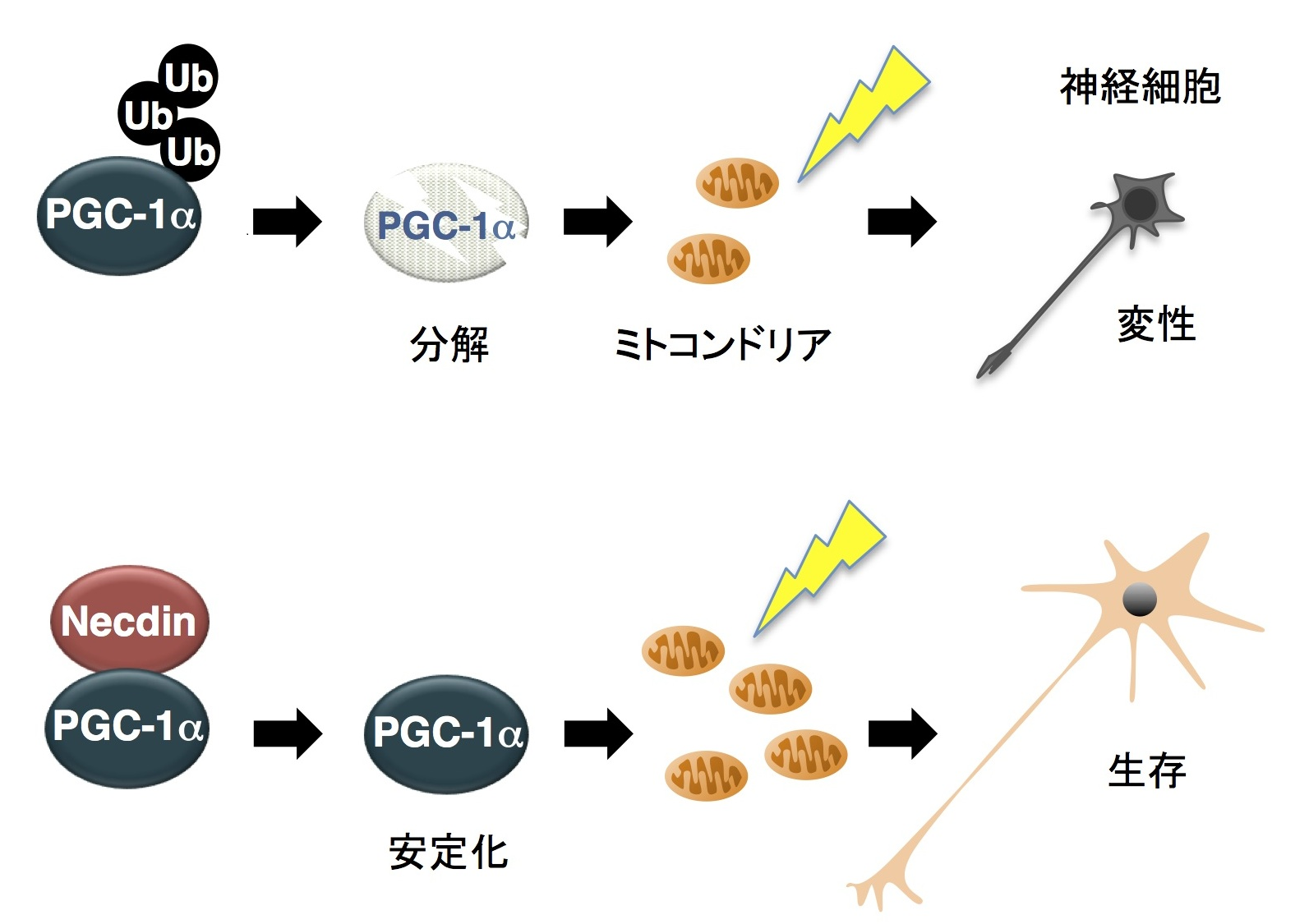
図 ネクジンはPGC-1αのユビキチン化 による分解を抑えてミトコンドリアを増やすことで神経細胞の変性を防ぐ。
本研究成果が社会に与える影響(本研究成果の意義)
本治療法はパーキンソン病の有効な治療法として大変期待されます。さらに、パーキンソン病以外の神経変性疾患もミトコンドリア障害によって生じることが知られているため、ネクジンがこれらの予防や治療法開発のターゲットになることが期待されます。
特記事項
本研究成果は「Nature Communications」電子版に3月14日(月)午前10時(英国時間)に掲載されました。
【論文タイトル】Promotion of mitochondrial biogenesis by necdin protects neurons against mitochondrial insults
【著者】Koichi Hasegawa, Toru Yasuda, Chinatsu Shiraishi, Kazushiro Fujiwara, Serge Przedborski, Hideki Mochizuki, and Kazuaki Yoshikawa
参考URL
論文掲載先(Nature Communications)
http://www.nature.com/ncomms/2016/160314/ncomms10943/full/ncomms10943.html
用語説明
- ネクジン
ネクジン(Necdin):
1991年に吉川教授の研究グループによって発見されたタンパク質で、哺乳動物の神経細胞に豊富に存在しており、様々なタンパク質に作用することによって神経細胞死を防ぐことが知られています。
- パーキンソン病
振戦(ふるえ)、動作緩慢、筋強剛(筋固縮)、姿勢保持障害(転びやすいこと)を主な運動症状とする進行性の神経変性疾患であり、発症は50~65歳に多く60歳以上における有病率は100人に約1人とされ決して稀な疾患ではありません。
- ミトコンドリア障害
ミトコンドリアは細胞でエネルギーとして使われるATPをつくる細胞内小器官。細胞の生存と死の制御にも関わっています。パーキンソン病は、黒質ドパミン神経細胞のミトコンドリア機能不全によって起こるものと考えられています。また、アルツハイマー病、ALS、ハンチントン舞踏病などの主要な神経変性疾患の原因としてミトコンドリアの異常が注目されています。
- PGC-1α
ミトコンドリアを構成するタンパク質やエネルギー代謝に関連する酵素などの遺伝子を活性化するタンパク質。運動、絶食、寒冷などの刺激によって細胞内のPGC-1αが増えると、ミトコンドリアの数と活性が増えます。一方、神経細胞内のPGC-1αが、どのように調節されているかは、ほとんどわかっていません。
- アデノ随伴ウイルス(AAV)ベクター
アデノ随伴ウイルス(AAV)は、RNAウイルスで、通常その複製はアデノウイルスの存在下で行われます。このウイルスを改変して作成されたAAVベクターは、増殖/非増殖のいずれの細胞にも遺伝子導入が可能です。特に神経細胞にも安全に遺伝子導入が可能で、すでにパーキンソン病などの遺伝子治療に使われています。
- ユビキチン化
タンパク質修飾の一種で、ターゲットのタンパク質にユビキチンタンパク質が付加される反応。多くの場合、ユビキチン自身も重合して鎖状になり、修飾されたタンパク質はプロテアソームと呼ばれる巨大な酵素複合体で分解されます。
