実験的トキソプラズマ不活化ワクチンがどのように効くかを解明
宿主タンパク質 p62を標的とした新たなワクチンの開発に前進
リリース概要
大阪大学微生物病研究所の山本雅裕教授(免疫学フロンティア研究センター兼任)らの研究グループは、p62 (ピー 62)と呼ばれる宿主分子 が、病原性寄生虫「トキソプラズマ」の実験的不活化ワクチン の免疫的効果発揮に重要な役割を果たすことを発見しました。
研究の背景
トキソプラズマはエイズや抗癌剤投与下にある免疫不全の大人で致死的な脳炎や肺炎を引き起こす病原体です。また、健康な妊婦が初感染すると胎児に垂直感染し流産や死産、さらには新生児がトキソプラズマに感染した状態で生まれ先天性疾患の原因ともなります。現在、ヒトで使用可能なトキソプラズマのワクチンは存在せず、マウスなどの実験動物を用いて不活化ワクチン開発のための基礎研究が進んでいます。
しかし、トキソプラズマ不活化ワクチンがどのようにして免疫的効果を発揮するのか、特にワクチンを投与された側の体内でどのような免疫反応が最初に起きることが重要なのかについては、よく分かっていませんでした。
本研究成果が社会に与える影響(本研究成果の意義)
本研究で、以下のことが分かりました。
①インターフェロン ガンマ刺激依存的な宿主タンパク質であるp62がトキソプラズマに蓄積すること
②トキソプラズマ感染細胞では、p62とインターフェロン ガンマ依存的にキラーT細胞 活性化能が高まること
③p62欠損マウス個体で、トキソプラズマ不活化ワクチン投与に対するキラーT細胞活性が著しく低下すること
本研究成果は、近年我が国においても症例報告が急増しているトキソプラズマ症に対して、p62という新たな分子を標的とした新規のトキソプラズマ不活化ワクチン開発戦略を提供できるものとして大いに期待できます。
特記事項
本研究成果は、米国の科学雑誌 『Cell Reports』 (10月 1日付け:日本時間10月 2日(金)午前1時)にオンライン掲載されました。
研究の詳細な説明
1.背景
寄生虫「トキソプラズマ」は、世界人口の約3分の1に感染しているとされる日和見病原体の一つです。免疫力が正常なヒトや家畜では問題となることはほとんどありませんが、免疫力が著しく低下しているエイズ患者、抗癌剤投与下にある者あるいは免疫抑制剤投与下にある臓器移植患者などにおいて、致死的な脳炎や肺炎を引き起こします。さらにトキソプラズマは妊婦が初感染であった場合に胎児に感染してしまい、感染の時期によっては流産・死産あるいは新生児が先天的な水頭症や脳の石灰化を伴ったまま生まれ、重い脳神経精神症状を患ってしまう先天性トキソプラズマ症の原因となったりします。近年のユッケや生レバー等の肉の生食やジビエ肉の流行など我が国における食の嗜好の変化に伴い、トキソプラズマに汚染された生肉に接する機会の増大により、本邦においても先天性のトキソプラズマ症の報告が増加傾向にあり、社会的な問題となっています(詳細については、先天性トキソプラズマ&サイトメガロウイルス患者会「トーチの会」のホームページ http://toxo-cmv.org/ を参照して下さい。)
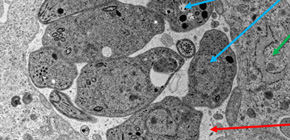
トキソプラズマ症に対しては、今のところ、ヒトで認可・使用されているワクチンは存在しません。現在、マウスなどの実験動物レベルでは、主要抗原の精製タンパク質を用いた実験的コンポーネントワクチン や、生きたトキソプラズマに放射線を照射し増殖能を失わせた不活化ワクチンの開発に向けた基礎研究が欧米を中心に進んでおり、それらを未感染マウスに投与することによってそれぞれトキソプラズマの抗原に特異的な抗体やキラーT細胞を誘導することが可能となってきています。トキソプラズマの不活化ワクチンを投与した時のキラーT細胞の活性化では、宿主(しゅくしゅ)細胞内に感染した際に形成する寄生胞 (図1) の中にトキソプラズマが分泌するタンパク質が最も優良な抗原となることが、米国のグループの先行研究により示されていましたが、寄生胞内に放出されたトキソプラズマ由来のタンパク質がどのようなメカニズムでキラーT細胞の抗原となるのかについては、ほとんど分かっていませんでした。
図1 「寄生胞」に包まれたトキソプラズマの電子顕微鏡写真
宿主の細胞の中に感染し、寄生胞内に存在しているトキソプラズマの電子顕微鏡写真
2.研究の手法と成果
大阪大学微生物病研究所の山本雅裕教授(免疫学フロンティア研究センター兼任)らの研究グループは、トキソプラズマの寄生胞にインターフェロン ガンマ依存的に蓄積する分子群の解析を以前から進めており、これまでにGBP などの寄生胞破壊因子 (2012年7月発表)やRabGDIα を介した制御機構(2015年8月発表)を報告してきました。その解析の中で、p62(およびユビキチン)と呼ばれる宿主分子群が寄生胞にインターフェロン ガンマ刺激依存的に蓄積することも見出していました( 図2 Aおよび 図4 )。インターフェロン ガンマ刺激によってトキソプラズマの殺傷に関与するGBPやRabGDIαなどと異なり、p62を欠損しても感染細胞内におけるトキソプラズマの数に変化はないことから (図2B) 、GBPやRabGDIαなどとは異なり、p62は寄生胞に蓄積するにもかかわらずトキソプラズマの殺傷には関与しないことが明らかとなりました。 以前に先行研究により、寄生胞内に放出されたトキソプラズマ由来の抗原がキラーT細胞の主要抗原になるということが明らかになったことから、山本教授らの研究グループはインターフェロン ガンマ刺激によってトキソプラズマ感染細胞を刺激した時のキラーT細胞の活性化を検討しました。その結果、未刺激の感染細胞に比べて、インターフェロン ガンマによって刺激した感染細胞では抗原特異的なキラーT細胞の活性が劇的に上昇することを見出しました (図3A) 。この感染細胞をインターフェロン ガンマ刺激した際に見られているキラーT細胞の強い活性化は、p62を欠損した感染細胞では有意に低下し (図3B) 、さらに個体レベルでも野生型マウスに比べて、p62欠損マウスではトキソプラズマの不活化ワクチン投与による抗原特異的なキラーT細胞の数が激減していました (図3C) 。
以上のことから、p62はインターフェロン ガンマ刺激に依存してトキソプラズマの寄生胞に蓄積し、寄生胞内に放出された抗原特異的にキラーT細胞の活性化を担うという、これまでに報告されていないユニークな役割を持っていることが明らかとなりました (図4) 。
3.今後の期待
本研究で山本教授らの研究グループは、トキソプラズマ寄生胞放出タンパク質特異的なキラーT細胞活性化におけるp62のユニークな機能を発見しました。山本教授らの発表とほぼ同時に独立して米国グループはヒトの細胞においてもインターフェロン ガンマ刺激的にp62がトキソプラズマ寄生胞に蓄積することを発見し、報告しており、今回の山本教授らの研究グループが発見した研究成果は、マウスのみならずヒトにも当てはまることが十分に予想されます。ワクチン開発が進まず、我が国を含め半ば「無視された感染症(Neglected Infectious Diseases)」の状態となっているトキソプラズマ症に対して、p62を新たな標的としその機能を高める等によって新規の治療・予防戦略を提供できることが期待されます。
掲載論文・雑誌
Lee Y, Sasai M, Ma JS, Sakaguchi N, Ohshima J, Bando H, Saitoh T, Akira S, Yamamoto M.
『p62 plays a specific role in interferon-γ-induced presentation of a Toxoplasma vacuolar antigen.』
Cell Reports.
2014年10月 2日(金)午前1時 オンライン掲載 (米国・東部時間: 10月 1日正午)
参考図
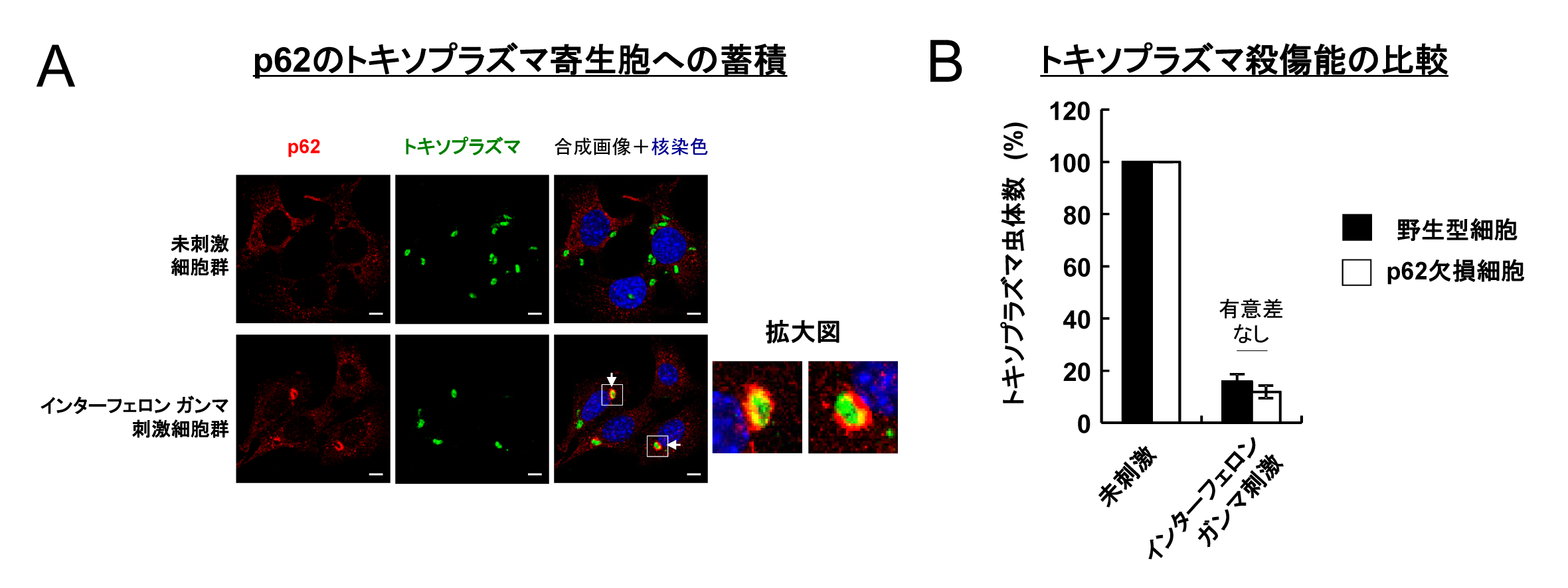
図2 p62はインターフェロン ガンマ刺激依存的に寄生胞に蓄積するが、殺傷能には関係ない
(A)p62 (赤色)がトキソプラズマ(緑色)と共局在していることを示す顕微鏡写真。(B)野生型細胞とp62欠損細胞を比較しても、インターフェロン ガンマ刺激後のトキソプラズマの虫体数は同様に低下している。すなわち、p62欠損細胞においてもインターフェロン ガンマ依存的殺傷は起きていることを示している。
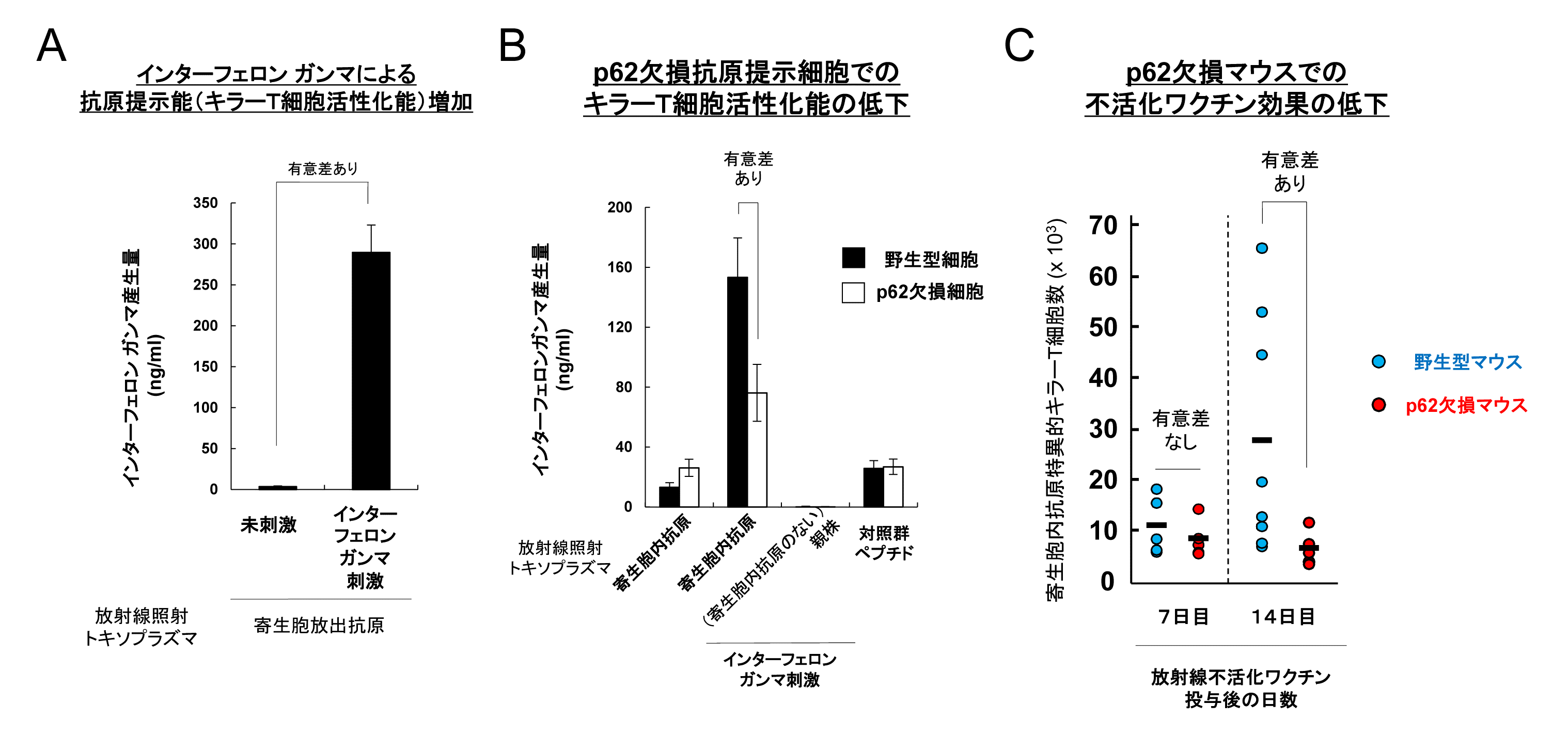
図3 p62欠損細胞およびマウスでは寄生胞内抗原に対する特異的キラーT細胞活性が低下する
(A)トキソプラズマに感染している抗原提示細胞である樹状細胞をインターフェロン ガンマで刺激すると、寄生胞内抗原特異的キラーT細胞に由来するインターフェロン ガンマの産生量(キラーT細胞の活性化の指標)が爆発的に増加する。(B)p62欠損した樹状細胞では(A)で見られたインターフェロン ガンマ刺激によるキラーT細胞の活性化が、野生型樹状細胞に比べて低下している。(C)放射線不活化したトキソプラズマを投与後、14日目の寄生胞内抗原特異的キラーT細胞数がp62欠損マウスではほとんど上昇していないことがわかる(すなわち、ワクチン効果が認められない)。
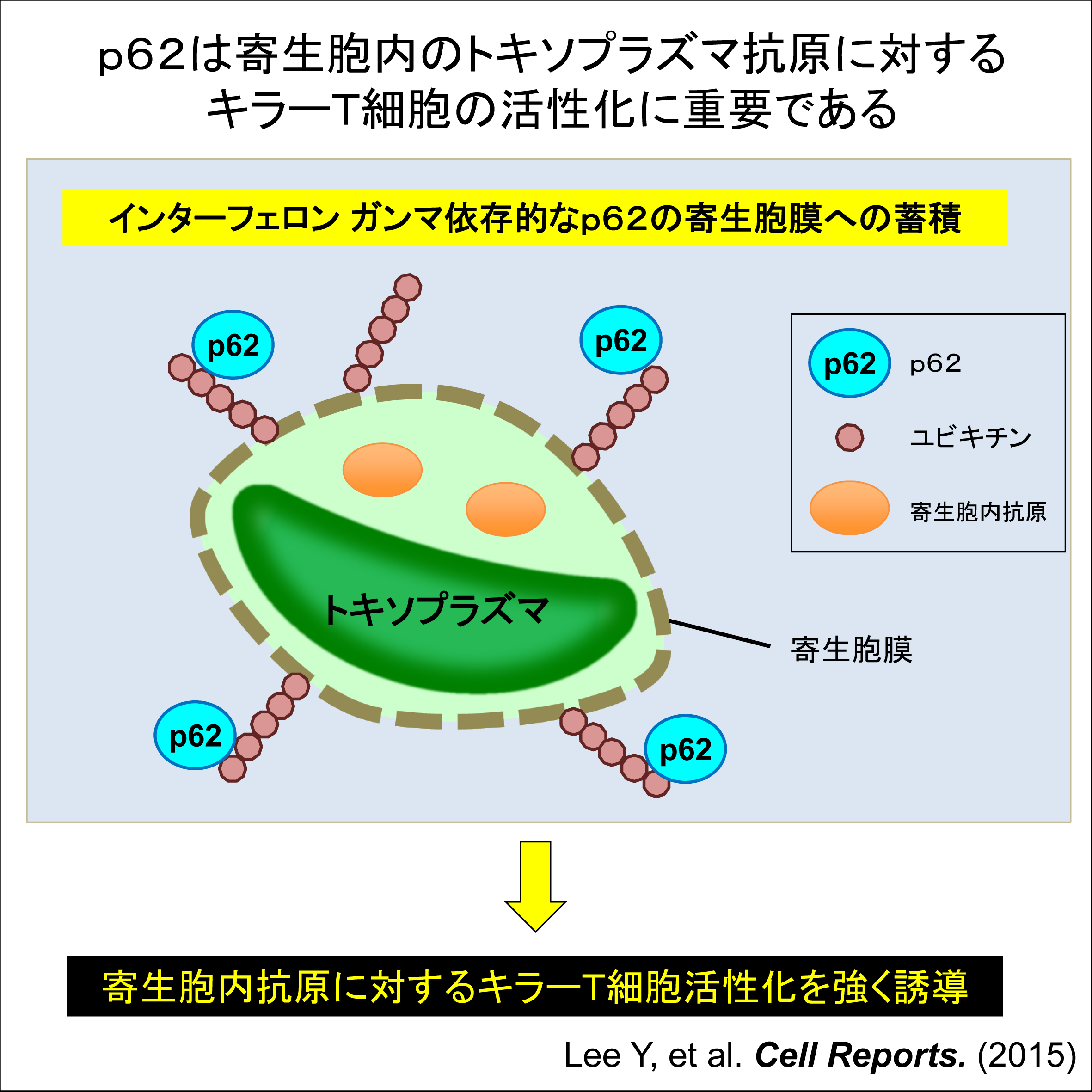
図4 p62による寄生胞内抗原特異的キラーT細胞活性化機構
トキソプラズマが感染した細胞内では、インターフェロン ガンマ刺激依存的に、まずユビキチンが寄生胞に蓄積し(今回の報道発表では詳細な説明は割愛しています)、p62が最終的に寄生胞膜に蓄積します。その結果、p62依存的に寄生胞内に溜まったトキソプラズマのタンパク質が処理され、キラーT細胞の抗原となっていると考えられます。
参考URL
論文掲載先(Cell Reports)
http://www.cell.com/cell-reports/fulltext/S2211-1247(15)01016-5
大阪大学免疫学フロンティア研究センター 山本研究室
http://www.biken.osaka-u.ac.jp/lab/immpara/
用語説明
- 宿主分子
宿主(しゅくしゅ)分子:
宿主の細胞に由来するタンパク質。
- 不活化ワクチン
予防接種などで投与されるワクチンのうち、死んだ細菌やウイルスを使用して作製されたワクチン
- インターフェロン
病原体、あるいはガン細胞に対して体内防御的に働くタンパク質。アルファ、ベータ、ガンマなどがあり、それぞれ免疫反応に重要な働きをする。
- キラーT細胞
免疫細胞の一種で、病原体あるいはウイルスに感染した自己細胞を殺傷する能力がある。
- 実験的コンポーネントワクチン
ウイルスや細菌の抗原成分のみを抽出してつくられたワクチン(実験動物に用いられる)
- 寄生胞破壊因子
トキソプラズマの寄生胞を抑制・破壊するタンパク質
- RabGDIα
トキソプラズマに対する宿主免疫反応を抑制するタンパク質の一つ(寄生胞破壊因子を阻害する)
- GBP
トキソプラズマ寄生胞の破壊を誘導するタンパク質群
