日本発!がん治療法の革新
世界最小クラスの核酸医薬デリバリーシステムを開発
本研究成果のポイント
・ 世界最小クラスの10nm (ナノメートル)サイズの遺伝子送達試薬の作成に成功
・ 十分な量の核酸をがん細胞に送達・集積させることができ、確実な抗がん作用が得られることを実証
・ 核酸の全身へのデリバリーツールとして、さまざまな新規治療薬への応用に期待
リリース概要
大阪大学大学院医学系研究科外科学講座(消化器外科学Ⅰ)の山本浩文准教授と呉しん大学院生(博士課程4年)の研究グループは、静注(静脈注射)可能な世界最小クラス:10nm(ナノメートル)サイズの遺伝子送達試薬:スーパーアパタイト の作成に成功し、飛躍的に効率よく固形がんに核酸を集積させることに成功しました。核酸は生体内では傷つきやすく、癌細胞に送達させることができる量は不十分でしたが、スーパーアパタイトを用いることで、核酸に傷がつかないうちに腫瘍の細胞質に送達させることができます。核酸の全身へのデリバリーツールとして、さまざまな新規治療薬への応用が考えられ、世界的に停滞している核酸医薬の新しい門戸を日本から開くことが期待されます。
本研究成果は、2015年3月4日(水)14時(米国東部時間)に、米国科学誌「PLOS ONE」のオンライン版で公開されました。
研究の背景
siRNAやmicroRNA等を用いた核酸医薬は、試験管内では切れ味よく分子の働きをコントロールできるので次世代の医薬品として期待されています。しかし、直接接触させることができる眼・皮膚や、比較的送達が容易な肝・腎疾患では臨床試験が進んでいますが、固形がんの治療、特に静注による全身治療の臨床利用は大きく遅れています。
本研究で開発した世界最小クラスのナノ粒子:スーパーアパタイトは、リン酸、炭酸、カルシウムという単純な組成から成り、マウスやカニクイザルでは顕著な副作用がみられませんでした。一方、抗アポトーシス遺伝子サバイビンを抑制する核酸をマウスに静注すると、皮下に埋め込まれた癌細胞にアポトーシスが誘導され、強い抗腫瘍効果を認めました。核酸はそのままでは血液中で分解されやすいため、生体では傷みやすくがん細胞に送達させることができる量はわずかですが、スーパーアパタイトを利用すると核酸に傷がつかないうちにがん細胞に大量の核酸を送達させることができます (図) 。
本研究成果が社会に与える影響(本研究成果の意義)
スーパーアパタイトは、核酸の全身へのデリバリーツールとして革新的な性能を有し、分子生物学的な知見の蓄積した今日においては、ほとんどの新規治療薬につながる可能性が考えられます。また肝・呼吸器疾患、炎症性疾患、ワクチン開発などにも発展応用できる可能性があり、世界的に停滞している核酸医薬の新しい門戸を日本から開くことが期待されます。
特記事項
本研究成果は、米国科学誌「PLOS ONE」のオンライン版にて公開されました(米国東部標準時 3月4日14時)。
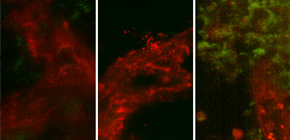
参考図

図 マウス皮下腫瘍の血管(赤)とがん細胞に取り込まれた核酸(緑)
スーパーアパタイトは、他の全身性DDS製剤よりも、がん細胞への核酸の取り込みが多いことがわかる。
参考URL
論文掲載先(PLOS ONE)
http://dx.plos.org/10.1371/journal.pone.0116022
用語説明
- スーパーアパタイト
pH応答性の遺伝子導入試薬である炭酸アパタイト(赤池敏宏主席研究員(公益財団法人国際科学振興財団)が2006年に開発)を微細粒子化して全身投与可能としたもので、静脈注射用の製剤。その優れた腫瘍集積性と高い抗腫瘍効果から、がんに対する治療剤としての特許性が付加されました。 【特許第5436650号 スーパーアパタイト超微細ナノ粒子 出願日:2012年11月28日、登録日:2013年12月20日】
