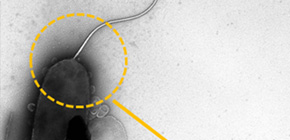
立って働き、しゃがんで休憩 細菌べん毛モーターは伸び縮みにより活性化
最新技術でも実現できない高性能ナノマシン「べん毛モーター」のしくみが明らかに
リリース概要
大阪大学大学院理学研究科の今田勝巳教授、名古屋大学大学院理学研究科の小嶋誠司准教授、本間道夫教授の共同研究グループは、これまで大きな謎だった細菌のべん毛モーターが活性化するしくみを明らかにしました。
べん毛モーターは、イオンの濃度差をエネルギー源とし、100%に近い高いエネルギー変換効率で高速回転するなど、現在の技術では人工的に実現できない高性能なナノマシンです。固定子 がモーターに組込まれる際に、折り畳まれていた固定子の一部が伸びて細胞壁に結合することで、モーターが活性化することが分かりました。その基本的作動原理の解明は、将来の活躍が期待される超高効率モーターやナノサイズのモーターの開発を目指す上で極めて重要です。
本研究成果は、2014年9月1日以降、米国科学誌「米国アカデミー紀要(Proceedings of the National Academy of Sciences)」のオンライン版で公開されます。
研究の背景
細菌は、べん毛と呼ばれるらせん状の繊維をスクリューのように回して水中を泳ぎます (図1) 。回転を駆動するのは、繊維の根元にあり細胞膜を貫通する直径約45ナノメートルの蛋白質でできた分子モーターです (図1) 。べん毛モーターは、細胞の外から内に流れるイオン流をエネルギー源とし、極めて高いエネルギー効率で作動します。大腸菌やサルモネラなどのモーターは、水素イオンを使って毎秒300回転(毎分1万8千回転)とF1エンジン並みの速度で回転します。また、海洋性ビブリオ菌のモーターは、ナトリウムイオンを使って毎秒1,700回転(毎分約10万回転)とジェットエンジンの回転数を遥かに超える速度で回ります。
イオンがモーターの固定子ユニット中を流れると、固定子と回転子リングの間に相互作用が生じて回転力が発生しますが、実際に回転するには固定子を回転力に負けないようにしっかり固定する必要があります。そのため、モーターの固定子ユニットには細菌の細胞壁に相当するペプチドグリカン層 に結合する領域があり、各固定子ユニットは回転子の周りに組込まれると細胞壁にしっかり固定されます。このとき固定子ユニットはイオンを流し始め、モーターが活性化します。べん毛モーターの固定子ユニットは約10個ですが、個々のユニットは回転中のモーターに組込まれたり外れたりして交換され、モーターから外れた固定子はイオンを流さなくなります。このように、固定子のモーターへの組込み・固定・イオン透過は連動していますが、固定子がモーターに組み込まれるメカニズムやモーターに組込まれたときにだけ細胞壁に結合してイオンを流すしくみは大きな謎でした。
手法と成果
共同研究グループは、海洋性ビブリオ菌のナトリウム駆動型べん毛モーターの固定子を構成するタンパク質の細胞壁に結合する部分(PomBc)に着目し、大型放射光施設Spring-8 で収集したX線回折データを用いたX線結晶構造解析法 により、分子構造を解析しました。」 (図2) 。明らかになったPomBcの構造は非常にコンパクトで、このままでは細胞壁に届かないことから、モーターに組込まれるときに大きく構造変化する必要があります (図3) 。構造をよく調べたところ、PomBcのN末側領域で分子が大きく伸び上るような構造変化が予想されました。そこで、この領域の様々な場所に生体内でジスルフィド架橋 をつくる変異を導入し、架橋により構造変化を妨害したり還元剤を加えて架橋を切断したりしたときに、モーターの回転・固定子のモーターへの組込み・イオン透過能がどうなるか調べました (図2) 。すると、PomBcのN末のヘリックスのN末側2/3の領域に架橋がかかるとモーターの機能が失われ、還元剤を加えると機能が回復し、還元剤を除くと再び機能が失われました。これらの結果から、PomBcのN末側で固定子の一部が伸び上がるような構造変化が起きて細胞壁に結合すること、この構造変化は可逆的であること(すなわち伸び縮みすること)がわかりました (図4) 。また、架橋が固定子のモーターへの組込みとイオン透過に影響しないことから、細胞壁へ結合する構造変化は固定子のモーターへの組込みとイオン透過が起きた後に起こることがわかり、べん毛モーターの活性化の順序が明らかになりました。
本研究成果が社会に与える影響(本研究成果の意義)
べん毛モーターは、イオンの濃度差をエネルギー源とし、100%に近い高いエネルギー変換効率で高速回転するなど、現在の技術では人工的に実現できない高性能なナノマシンです。その基本的作動原理の解明は、将来の活躍が期待される超高効率モーターやナノサイズのモーターの開発を目指す上で極めて重要です。また、細菌の病原性と運動性は密接な関係にあります。コレラ菌、魚介類の食中毒の主因である腸炎ビブリオ、人食いバクテリアとして知られるビブリオバルニフィカスといった、ビブリオ菌の仲間はもちろんのこと、他の病原菌においても、運動性が細菌の病原性の鍵を握る例が知られ、運動性の理解と制御は細菌学の中心課題のひとつです。今回の成果は、運動性から病原菌をコントロールするという面からも重要な成果です。
特記事項
本研究は、科研費新学術領域研究「少数性生物学」および「運動マシナリー」の一環として行われました。また、本研究は大阪大学と名古屋大学との共同で行ったものです。
掲載論文・雑誌
論文タイトル:
Conformational change in the periplamic region of the flagellar stator coupled with the assembly around the rotor.
(回転子周囲への集合と連動した、べん毛モーター固定子のペリプラズム領域の構造変化)
掲載誌: Proceedings of the National Academy of Sciences (PNAS)
参考図
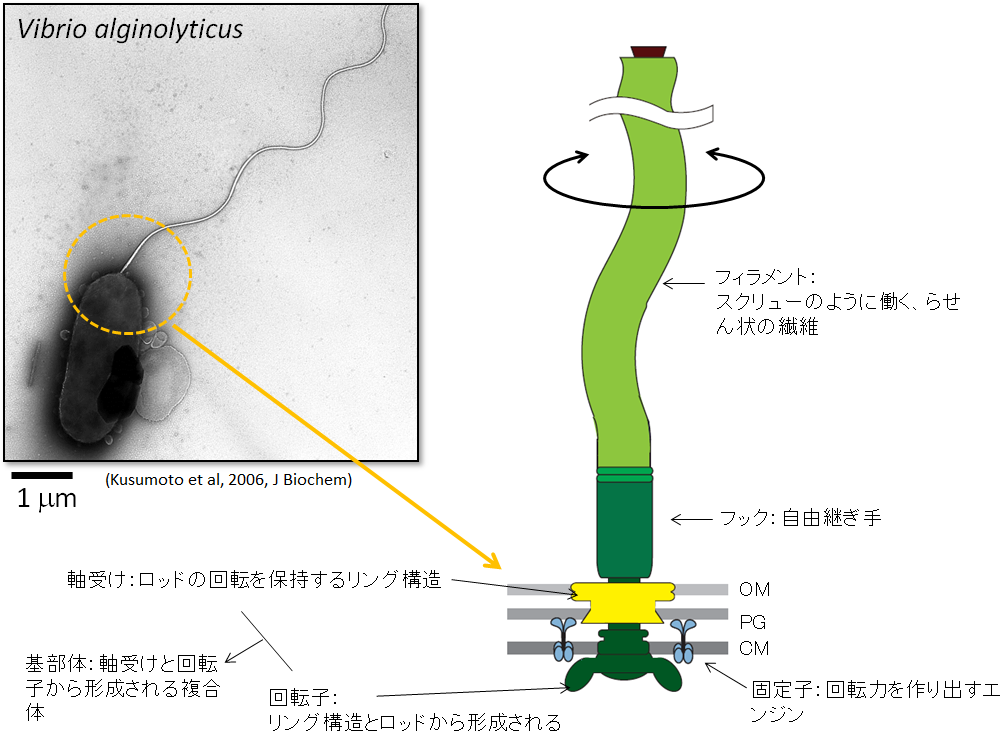
図1 ビブリオ菌の電子顕微鏡写真と細菌べん毛の模式図
ビブリオ菌は細胞の端に一本のべん毛を持ち、スクリューのように回転させて泳ぐ。回転力を作り出すエンジンはべん毛の根元に存在し、回転モーターの本体である固定子と回転子、回転子の回転を保持する軸受け、自由継ぎ手として働くフック、スクリューのように動くフィラメントで構成される。また、回転子と軸受け部分は基部体と呼ばれる。電子顕微鏡写真のスケールバーは1mm。OM、PG、CMは、それぞれ外膜、ペプチドグリカン層(細胞壁)、細胞膜を示す。
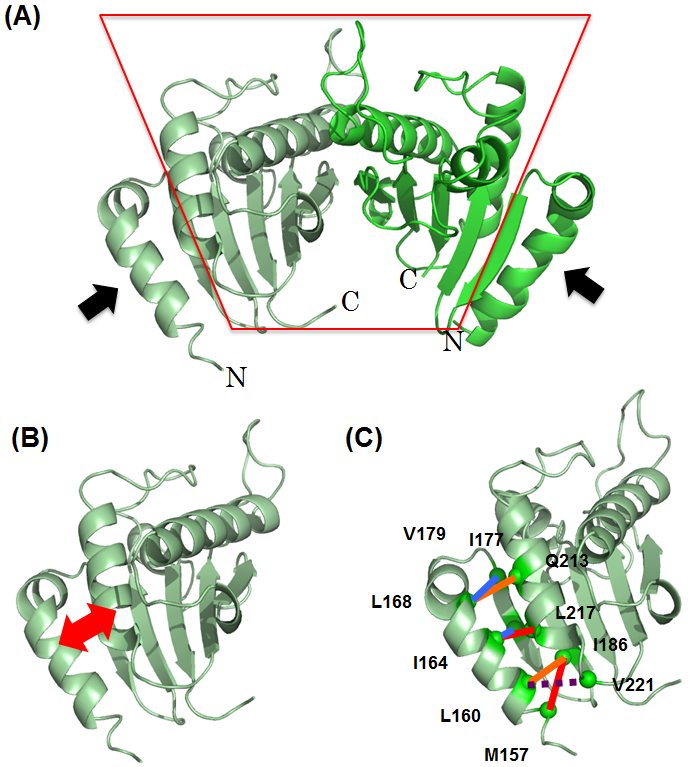
図2 PomBcの分子構造
(A)解析したPomBcの構造。2つのPomBc分子が2量体を形成する。赤で囲った領域は細胞壁に結合する部分、黒い矢印は構造変化が予想される領域。N、CはそれぞれN末端とC末端を表す。
(B)赤矢印で示した部分の間を架橋でつなぎ、構造変化を妨げる実験を行った。
(C)架橋したアミノ酸のペア。青い線で示した残基を架橋してもモーターは機能するが、赤い線で示した残基を架橋するとモーターは機能しなくなる。オレンジの線で示した残基どうしは一部に架橋がかかり、一部のモーター機能が失われた。点線の残基どうしは架橋がかからず、モーターは機能した。
従って、(A)で黒矢印で示したN 末のヘリックスのN 末側から2/3 の領域を架橋により固定すると、モーター機能は失われる。
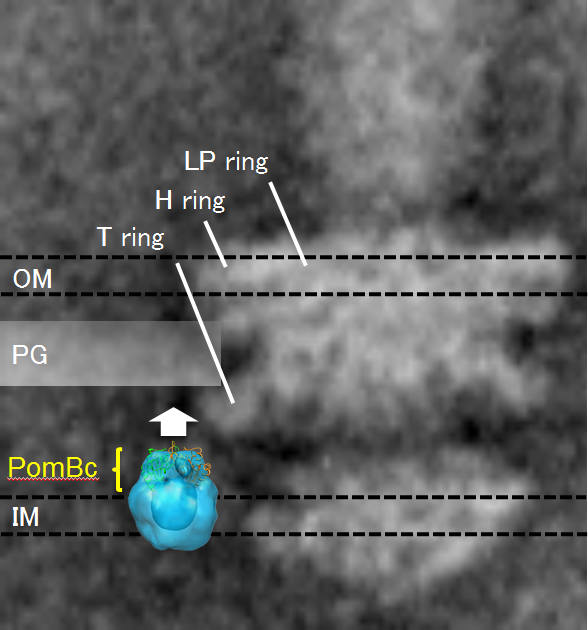
図3 固定子の位置と大きさの比較
固定子の電子顕微鏡像にPomBcの構造を当てはめ、べん毛基部体の電子顕微鏡像と共に表示。OM、PG、CMは、それぞれ外膜、ペプチドグリカン層(細胞壁)、細胞膜を示す。この構造のままでは、PomBc部分はペプチドグリカン層(細胞壁)に届かない。白矢印で示した方向に伸びる必要がある。
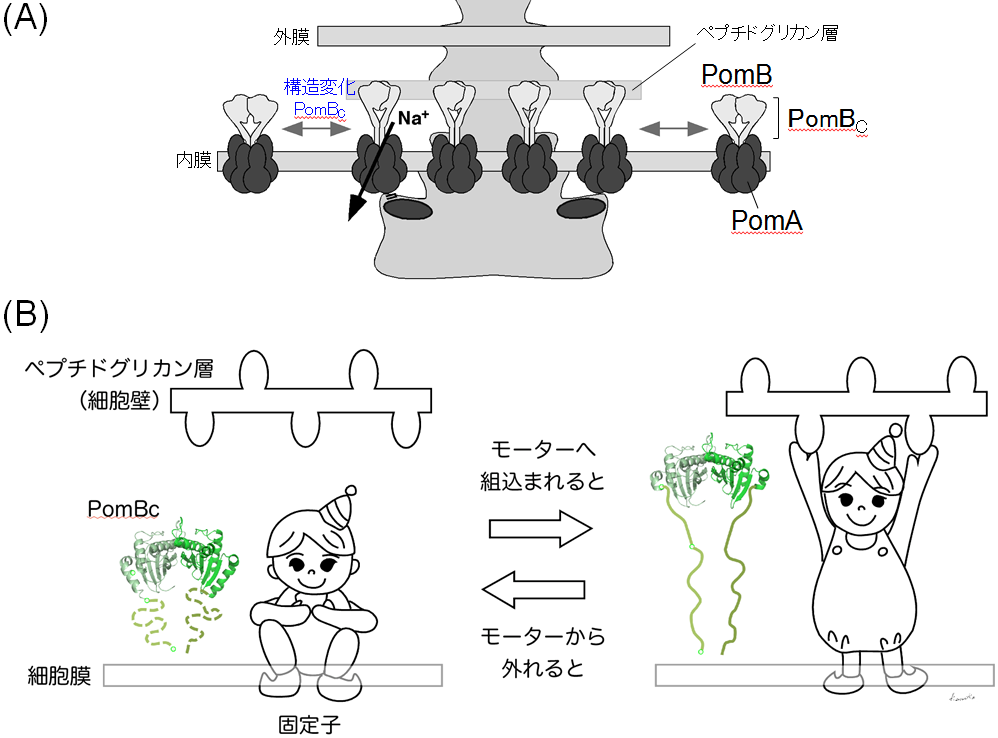
図4 モーターへの組込みに伴う固定子の構造変化モデル
(A)構造変化の模式図。
(B)構造変化のイラスト図。
固定子がモーターに組込まれると、PomBc部分が立ち上がるような構造変化を起こし、細胞壁に結合する。モーターから外れているときはしゃがんだような構造になり、細胞壁に届かないため、細胞壁に結合せずに細胞膜上を自由に移動する
参考URL
用語説明
- 固定子
モーターの中で、回転する部分を回転子、固定されて動かない部分を固定子と呼ぶ。モーターを作動させると回転子と固定子の間で力が働くが、固定子が固定されているので回転子の方が回る。べん毛モーターでは、固定子はイオンの通り道でもあり、イオンの濃度差を回転力に変える働きの中核を担っている。
- ペプチドグリカン層
ペプチドと糖が結合してできた複雑な生体高分子。細菌の細胞内膜の外側をくるむ細胞壁の主成分である。
- 大型放射光施設SPring-8
電子を光速近くまで加速し、磁石で曲げたときに出る光を用いて、さまざまな解析に利用するための実験施設。強力なX線を発生させることができるため、X線を使ったいろいろな研究が行われている。
- X線結晶構造解析法
物質の立体構造を原子レベル調べる方法。X線を結晶に照射し、その回折パターンから立体構造を決定する。
- ジスルフィド架橋
蛋白質を構成するアミノ酸残基のひとつであるシステインはスルフィドリル基をもち、もうひとつのシステインがある近くにあるとスルフィドリル基どうしで共有結合(ジスルフィド結合)を作り、つながってしまう(架橋)。この結合は酸化状態では結合し、還元状態では切れるので、蛋白質のさまざまな性質を調べるために使うことができる。
