その名は「メチロー」エピジェネティクスを生きたまま可視化できるマウス作成
発生・幹細胞研究、抗がん剤などの創薬研究の進展に大いに期待!
本研究成果のポイント
・エピジェネティクス はDNA配列の変化を伴わないで細胞の個性が生み出される仕組み
・その代表格であるDNAメチル化の時々刻々と変動する様子を顕微鏡で捉えられるマウスの作製に成功
・このマウスの開発によって、発生・幹細胞研究や、抗がん剤などの創薬研究などが大いに進展することが期待
リリース概要
大阪大学微生物病研究所の上田潤特任助教、山縣一夫特任准教授らのグループは、エピジェネティクスの代表格であるDNAのメチル化をマウス個体の全身の細胞において生きたまま可視化することに成功し、このマウスを「メチロー(MethylRO:methylation probe in ROSA26 locus)」と命名しました。DNAのメチル化は、遺伝子の転写活性の制御に関わっており、それが様々な細胞で時々刻々と変化することにより、正常な発生やがん化の過程などにも関与しています。ところが、これまではこの変化を静止画(スナップショット)としてしか捉えることができませんでした。しかしこのマウスの開発によって、DNAのメチル化がどのように変動するのかを生きたまま個体レベルで追跡し、評価することができるようになりました。このことからメチローマウスは発生・幹細胞研究はもとより、抗がん剤などの創薬開発にも極めて有用であると考えられます。
研究の背景
DNAのメチル化は、4つのDNA塩基、アデニン、シトシン、グアニン、チミンのうち、シトシンがメチル化される化学修飾であり、それは通常のシトシンとは機能的に異なる性質を持つことから、「第5の塩基」とまで呼ばれています。その機能としては、高度にメチル化された遺伝子領域の転写活性を抑制する働きがあり、遺伝子刷り込み(ゲノミックインプリンティング)やX染色体の不活性化、トランスポゾンなどの動く遺伝子の抑制などに関与しています。DNAのメチル化は正常な発生過程に重要であることはさることながら、その制御異常が発がんなどの様々な疾患と関連していることもよく知られており、DNAのメチル化を指標とした抗がん剤の開発も進められています。また、妊婦の生活習慣が胎児のDNAのメチル化状態に影響を及ぼし、ひいては生まれてくる子どもの疾病罹患率に影響を及ぼすとの研究報告もあり、ストレス応答や環境の変化によってもDNAのメチル化に代表されるエピジェネティクスがダイナミックに変化するものとして認識されるようになってきました。しかし、バイスルファイト処理、免疫組織化学、免疫沈降法などの従来の実験手法では細胞を変性処理してしまうことから、ある一時期のDNAのメチル化状態しか解析できませんでした。このため、これらのエピジェネティクスの動態変化を追跡する手法の開発が求められていました。
本研究ではメチル化DNAを認識するMBD1(Methyl-CpG Binding Domain protein 1)たんぱく質のMBDドメインに赤色蛍光たんぱく質を融合した蛍光プローブを作製し、この遺伝子をジーンターゲッティング法によって全身で遺伝子発現することが知られているROSA26遺伝子座にノックインすることで、マウスの全身でこのプローブを発現した遺伝子改変マウスを開発しました (図1) 。そしてこのレポーターマウスより得られた細胞を、山縣一夫博士らが独自に開発した低侵襲性ライブセルイメージング技術と組み合わせることによって、マウスの着床前初期胚発生過程 (図2) 及びES細胞の樹立過程の長期間ライブセルイメージングに成功しました。さらに画像データの解析から、細胞分化が進行するに伴って特にセントロメアと呼ばれる遺伝子領域のDNAメチル化が上昇し、かつヘテロクロマチン構造が形成されていく様子 (図3) を捉えることにも世界で初めて成功しました。これらの結果から、核内のDNAのメチル化パターンが細胞分化や細胞の病態の指標になり得ることを示しました。
本研究成果が社会に与える影響(本研究成果の意義)
これまでは細胞を変性処理することによってしか解析できなかったDNAのメチル化が、生きたマウス個体において可視化できるようになり、各種細胞における時系列的な変化を解析できるようになったことに本研究成果の大きな特色があります。
今後は、本研究成果を用いることによって、ほ乳類の発生・分化過程はもとより、発がんなどの病態進行過程においてDNAのメチル化ならびにそれが集積するヘテロクロマチン構造がどのように変化するかを解析することが可能になると考えます。メチローマウスを他のレポーターマウスと掛け合わせて発生・幹細胞研究に活用することで生命現象の解明に貢献したり、抗がん剤などの創薬スクリーニングに活用することでバイオ産業の発展に貢献したりすることも期待されます。さらに、iPS細胞を樹立する過程でDNAのメチル化が大きく変動することが知られていますが、本リソースを用いることによってその過程をイメージングすることも可能となり、細胞のリプログラミング過程を理解する上でも有用なツールとなることが期待されます。
特記事項
本研究は文部科学省科学研究費補助金、新学術領域「動的クロマチン構造と機能」(代表・胡桃坂仁志・早稲田大学教授)の支援のもと行いました。また、本研究は九州大学・医学研究院の大川恭行准教授のグループ、大阪大学・生命機能研究科の木村宏准教授のグループ、ならびに扶桑薬品工業株式会社の八尾竜馬主任研究員との共同で行ったものです。
本研究成果は、2014年6月3日に米国Cell pressの科学誌「Stem Cell Reports」のオンライン版で公開されます。
参考図

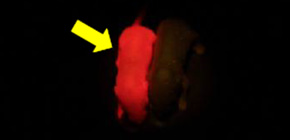
図1 DNAのメチル化を可視化したメチローマウスの新生児(黄矢印)
励起光を照射してフィルターを介して見ると全身が赤く光ります(右図)。

図2 メチローマウスを用いた着床前初期胚発生過程のライブセルイメージング画像
2細胞期受精卵から胚盤胞期までの約4日間、核内のメチル化DNAの変化を安定して観察できるようになりました。
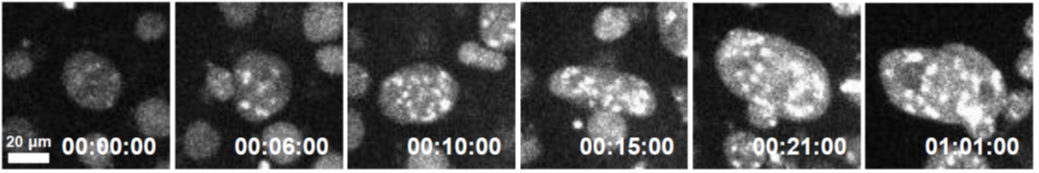
図3 細胞が分化する過程でのメチル化DNAの変化を捉えた画像
受精卵から胎盤の細胞ができていく過程で、核内においてDNAメチル化が上昇し、ヘテロクロマチンが形成されてゆく様子がわかります。
参考URL
大阪大学微生物病研究所 附属生体応答遺伝子解析センター
http://www.cgabr.biken.osaka-u.ac.jp/index.php
用語説明
- エピジェネティクス
我々の体を構成する細胞は同じ遺伝情報(ゲノムDNA)を持っているにも関わらず、機能の全く異なる200種類以上の細胞に分化することが知られています。このように、遺伝情報の変化を伴わないで細胞の個性が生み出される仕組みはエピジェネティクスと呼ばれています。
