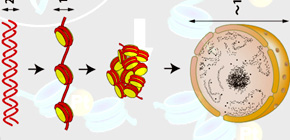
DNAを有害な放射線から守る新しい仕組みがわかった
放射線の影響の理解や、がん治療への応用につながる
本研究成果のポイント
・ゲノムDNAは放射線で損傷(切断)を受けるが、DNA密集箇所で、損傷から守られることを発見した。
・放射線とDNA損傷の関係を定量的に突き止め、そのメカニズムを明らかにした。
・放射線(ガンマ線、重粒子線)や化学物質によるがん治療の効率を上げる仕組みを見出した。
リリース概要
放射線は生物にとって大きな脅威。放射線にさらされると細胞内のDNAが切断され、遺伝子が正しく機能しなくなったり、がん化や細胞死が引き起こされたりするからです。しかし、自然界にはもともと自然放射線が存在しています。私たちのDNAは損傷被害を受けないのでしょうか?
今回、大阪大学の髙田英昭助教(元・国立遺伝学研究所研究員)と国立遺伝学研究所の前島一博教授は、同研究所・花房朋研究員、大阪府立大学・森利明准教授、国立国際医療研究センター・志村まり室長、東レリサーチセンター・飯田豊部長、放射線医学総合研究所・石川顕一研究員、同志社大学・吉川研一教授、立命館大学・吉川祐子客員教授らと共に、生物が放射線からDNAを守る新たな仕組みを突き止めました。それは、DNAが密に集まる、ということでした。DNAは特殊な構造をした長い線維で、細胞の核の中に折りたたまれています。そうしたDNAが、密に集まって存在(凝縮)するか、散らばって存在するかが、放射線による損傷の程度に大きく影響していたのです( 図1 )。髙田助教と前島教授らは、DNAの凝縮と放射線耐性の関係を、定量的に示すことに成功しました。さらに、その解析結果を用いてコンピュータシミュレーションを行い、放射線がDNAを切断するメカニズムも詳しく明らかにすることができました。
その結果、自然界から浴びる放射線を、生物は細胞中のゲノムDNAを凝縮させることで、日々防御していることがわかりました。生物がDNAを放射線から守ろうとする新たな仕組みを明らかにした今回の研究成果は、がん治療など医療応用の面でも、重要な基礎知識を提供するものです。
生物にとって有害な放射線ですが、がん治療においては、がん細胞を死滅させるために有効に利用されています。今回の成果は、DNAの凝縮を弱める薬を併用することで、がんの放射線治療(ガンマ線治療、重粒子線治療)や化学療法の飛躍的な効果向上が期待できることを意味しています。
研究の背景
私たちの体を構成する1個1個の細胞の中には、全長約2メートルにもおよぶDNA が収められています。DNAは直径2ナノメートル のとても細い糸で、ヒストンと呼ばれるタンパク質に巻かれてヌクレオソームと呼ぶ線維構造( 図2 )を形成していることが知られています。細胞核中では、このヌクレオソーム線維が塊を形成し、他のタンパク質と共に「クロマチン」( 図2 )として収められています (Proc Natl Acad Sci USA (2008) 105: 19732–19737; EMBO Journal (2012) 31: 1644-53 などに発表)。
地球上の生物は、毎年約2.4ミリシーベルトの放射線を自然界から浴びています。放射線はDNAの切断を引き起こすので、これは、生物の生死にかかわる深刻な問題です。DNAが集まって凝縮している状態が保たれていることは、放射線などの環境ストレスからゲノム情報を守っているのではないかと以前から推測されていました。実際、DNAの凝縮とDNA損傷の関係について調べた研究が過去にも報告されています。しかしながら、損傷を加えず長いDNAを扱う方法やDNA損傷を高感度かつ定量的に検出する良い方法が無かったことから、これまでは厳密な検証ができませんでした。
研究の詳細
今回、髙田英昭助教(大阪大学)と前島一博教授(国立遺伝学研究所)は、DNAの凝縮状態を自在に変化させることができ、さらにDNA損傷を定量的に検出できるシステムを構築しました( 図3 )。
DNA損傷を定量的に解析することがこれまで困難だった大きな理由は、ピペッティングなどの実験操作により、DNAに物理的損傷が加わってしまい、放射線の影響のみを厳密に定量することができなかったからです。そこで今回、髙田助教らは、DNAが含まれる核をヒトの培養細胞(HeLa細胞)からそのまま取り出し、うすいガラス(カバーガラス)の上に貼り付けるという方法を採用しました。DNAは核の中で保護されています。核を貼り付けたままのカバーガラスをいろいろな反応溶液に浸すことで、実験操作にもとづくDNAへの物理的損傷を避けるようにしたのです。
核のなかのDNAの凝縮状態を変化させるには、二価陽イオンであるマグネシウムイオン(Mg 2+ )を用いました。DNAの構造単位に含まれるリン酸基は負電荷を帯びているため、リン酸基の負電荷同士には反発し合う力が働き、DNAを凝集しにくくさせています。そこで、二価陽イオンであるマグネシウムイオン(Mg 2+ )を加えることによって、DNAに含まれる負電荷を打ち消し、密に凝縮した状態を誘導することができます。一方、これにEDTAという薬剤を加えると、マグネシウムイオンが取り除かれて陽電荷が打ち消され、DNAの負電荷が元に戻り、DNAは凝縮しなくなります(分散します)。実際には、DNAは核の中でヒストンや他のタンパク質と共に、「クロマチン」と呼ばれる構造を作っています( 図2 )。
このように、マグネシウムイオンの濃度の異なる溶液にカバーガラスに貼り付けた核を移すことによって、クロマチンの凝縮状態を変化させた核を用意しました。それに、放射線(ガンマ線)照射し、DNA切断がどのくらい起こっているかをTUNELアッセイ により検出しました( 図4 )。DNA切断は、蛍光色素のシグナルとして検出されるので、それを高性能CCDカメラで測定しました。実験操作を通じて、核はカバーガラス上に保持されたままなので、作業過程による物理的なDNA損傷を最低限に抑えることができました。なお、高線量の放射線照射は、大阪府立大学の森利明准教授の協力の下に行いました。低線量の放射線照射は、国立遺伝学研究所の放射線照射施設で行いました。また重粒子線の照射は放射線医学総合研究所・石川顕一研究員と行いました。
DNA損傷を定量的に解析した結果は、驚くべきものでした。DNA損傷はクロマチンの凝縮状態の違いに非常に敏感でした。細胞の間期の核における凝縮状態では、凝縮していない状態に比べて16倍もの放射線耐性を得ることができました。細胞の分裂期のきわめて高度に凝縮した状態のクロマチンでは、凝縮していない状態に比べて50倍もの放射線耐性を得ることができました。
では、なぜクロマチンが凝縮していると、DNA損傷を抑えることができるのでしょうか?放射線によるDNA損傷の主な原因は、放射線によって水分子が開裂することにより発生するヒドロキシルラジカル(・OH) だと考えられています。実際に、ラジカルの発生を抑制するラジカルスカベンジャーの存在下では、クロマチンが凝縮していなくても(分散していても)、DNA損傷はほとんど検出されませんでした。ヒドロキシルラジカルの寿命は短いので、DNAと離れた場所で発生してもDNAに損傷を与えることはできません。もし、クロマチンが凝縮していると、DNAの周りの水分子の数が少なくなるため、放射線を照射したときにDNAの周りで発生するヒドロキシルラジカルの数は少なくなります。これが、クロマチンが凝縮するほど高い放射線耐性が得られる理由だと考えられます。
クロマチンが凝縮することでDNAを保護することができるのは放射線(ガンマ線)からだけではありません。放射線医学総合研究所の石川顕一研究員とともに、重粒子線がん治療装置(Heavy Ion Medical Accelerator in Chiba:HIMAC) を用いて間期核のクロマチンに対して重粒子線を照射したところ、クロマチンが凝縮することでDNA損傷を抑制することがわかりました。また、国立国際医療研究センターの志村まり室長、東レリサーチセンター・飯田豊部長とともに、抗がん剤として用いられているシスプラチン のDNAへの結合量を誘導結合プラズマ質量分析計(ICP-MS) によって調べたところ、クロマチンが凝縮することでシスプラチンのDNAへの結合量が減少することがわかりました。このように、クロマチンが凝縮することでDNA損傷を防ぐという性質は、放射線に限ったものではなく、クロマチンが持つ一般的な性質であることを見出しました。
本研究の意義
間期の核内でもクロマチンはある程度凝縮した状態を保っていますが、今回の研究によって、その生物学的意義が明らかになりました。生物は、DNAを凝縮させることで、遺伝情報であるDNAが損傷を受けることを防ぐという仕組みを備えていたのです。生物には損傷したDNAを修復する機構も備わっていますが、生物進化の初期のDNA修復機構が未発達な段階では、DNAを凝縮させて環境ストレスから守ることは特に大きな利点を持っていたと想像されます。また、真核生物では次世代に伝える重要な遺伝子情報を安全に維持するために、この仕組みを役立てていると思われます。例えば、私たちヒトの卵母細胞は約40年もの間、減数分裂の途中で停止しており、DNAを染色体の状態で高度に凝縮した状態に保っています。
今回の成果から、新たながん治療法を確立するためのヒントも得られました。クロマチンの凝縮をゆるめることで、がん治療に用いられている重粒子線や抗がん剤であるシスプラチンに対するDNAの感受性が増加することがわかりました。このことを利用して、クロマチンの凝縮をゆるめる働きがあるヒストン脱アセチル化酵素阻害剤(TSA)などを用いてがん細胞のクロマチンの凝縮をゆるめ、従来行なわれてきた放射線、重粒子線や抗がん剤を用いたがん治療の効率を飛躍的に向上させることが期待されます。
特記事項
本研究成果は、大阪大学 髙田英昭助教(元・国立遺伝研研究員)、国立遺伝学研究所 前島一博教授・花房朋研究員、大阪府立大学 森利明准教授、国立国際医療研究センター 志村まり室長、東レリサーチセンター 飯田豊部長、放射線医学総合研究所 石川顕一研究員、同志社大学 吉川研一教授、立命館大学 吉川祐子客員教授によっておこなわれた共同研究です。
JST・CREST「コヒーレントX線による走査透過X線顕微鏡システムの構築と分析科学への応用」、内藤記念科学振興財団、国立遺伝研・共同研究(A)の支援を受けました。
本研究成果は、2013年10月9日(日本時間10月10日)付の米科学誌PLOS ONEにオンライン先行掲載されます。
論文名:「Chromatin compaction protects genomic DNA from radiation damage」(クロマチンは凝縮することで放射線による損傷からゲノムDNAを保護する)
著者名:Takata, H., Hanafusa, T., Mori T., Shimura, M., Iida, Y., Ishikawa, K., Yoshikawa, K., Yoshikawa, Y., Maeshima, K.
doi: 10.1371/journal.pone.0075622
参考図

図1 DNAが凝縮していないときは、DNA(赤線)は放射線によって発生するヒドロキシルラジカル(活性酸素、・OH)や抗がん剤(青丸、Pt)による損傷を受けやすいが、凝縮しているときには、DNAはこれらから保護される。

図2 直径2ナノメートルの細い糸であるDNA(1段目)は糸巻きの役割をするヒストンに巻かれて、直径約11ナノメートルのヌクレオソーム(2段目)をつくる。前島教授らは最近、ヌクレオソームが不規則に折りたたまれてクロマチンを形成し(3段目)、細胞内に収められていることを突き止めた。
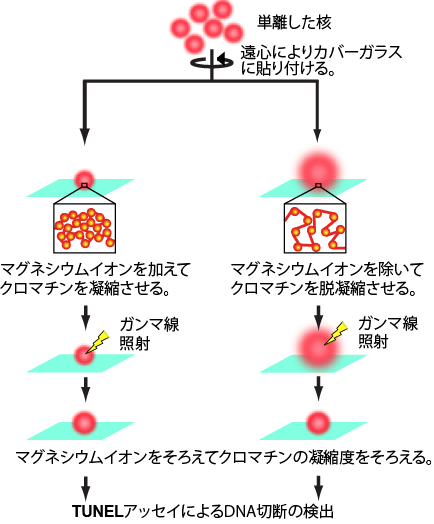
図3 DNA損傷を定量的に解析するために開発したシステム。
ヒト培養細胞から単離した核をカバーガラスに貼り付け、その後の実験操作はすべてカバーガラス上で行うことでDNAの物理的な損傷を最小限に抑え、定量的なDNA損傷の解析を可能にした。なお、クロマチンが脱凝縮すると体積が拡大するが、DNA切断を測定する際には、単位体積あたりの切断を測定するため、DNAの凝集状態をそろえた。
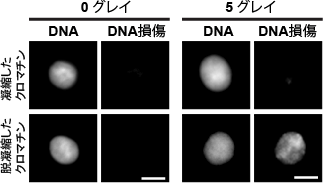
図4 0グレイと5グレイの放射線を照射したときのDNA損傷をTUNELアッセイによって検出した結果を示す。
5グレイの放射線を照射すると、クロマチンが凝縮していないときには明るいDNA損傷のシグナルが検出されるが、凝縮しているときにはほとんど検出されない。スケールバーは10マイクロメートルを示す。
参考URL
国立遺伝学研究所 構造遺伝学研究センター 生体高分子研究室
http://www.nig.ac.jp/section/maeshima/maeshima-j.html
大阪大学大学院工学研究科 生命先端工学専攻 生物工学コース 細胞動態学領域
http://www.bio.eng.osaka-u.ac.jp/cl/top.php
用語説明
- DNA
DNA(デオキシリボ核酸):
DNAは、生命の設計図であり、2本のごく細い鎖が、同じ軸を中心にらせんをまいた構造をしています。2本の鎖には、遺伝暗号となる「塩基対のはしご」がかけられています。二重らせんの直径は約2ナノメートルで、DNAを伸ばすと、全長はヒトで2メートルにおよびます。このようなDNAは、細胞が分裂する際に、切れたり絡まったりしないように、46本の束に分けられて染色体をかたちづくり、複製を経て新しい細胞(娘細胞)に分配されます。
- ナノメートル
1メートルの10の9乗分の1(10 -9 )。
- TUNELアッセイ
Terminal deoxynucleotidyl transferase dUTP Nick End Labeling assayの略称。DNAの2本鎖切断が生じた部位のDNAの3’末端にヌクレオチドアナログであるEdUTPを酵素反応で取り込ませます。DNAの損傷部位に取り込まれたEdUTPは蛍光標識されえた試薬と反応するため、蛍光顕微鏡でDNA損傷を蛍光シグナルとして検出することが可能になります。
- ヒドロキシルラジカル
放射線によって水分子が解裂することによって生じる活性酸素の一種です。寿命は100万分の1秒と短いが、非常に強力な酸化作用を示し、DNAをはじめとする生体分子に損傷を与えます。
- 重粒子線がん治療装置
炭素原子を高速に加速することで発生させます。身体表面から特定の深さで大量の線量を与え、その前後に与える線量が少ないため、がんに集中的に照射して正常組織への影響を最小限に抑えることが可能です。
- シスプラチン
化学式ではCl 2 H 6 N 2 Ptと表記されます。DNAと結合し、DNA分子間もしくは分子内で架橋を形成することでDNA複製を阻害し、細胞増殖を停止させます。代表的な抗がん剤の一つです。
- 誘導結合プラズマ質量分析計(ICP-MS)
試料に含まれる元素をプラズマによりイオン化し、質量分析計により微量元素も定量することが可能です。今回の研究では、細胞中のシスプラチンに含まれている白金を定量しています。
