免疫難病の発症機構の解明に1つの鍵
IL-6の異常産生に関わる分子の発見
リリース概要
免疫学フロンティア研究センター(WPI-IFReC)の増田和哉研究員(日本学術振興会)、岸本忠三教授(元大阪大学総長)らの研究グループは、数々の自己免疫疾患の発症機構解明につながる分子を発見しました。
研究の背景
関節リウマチをはじめとして多くの自己免疫疾患では患者の血液中に炎症性サイトカインIL-6の顕著な増加(異常産生)が認められます。IL-6受容体に対する抗体(トシリズマブ、商品名アクテムラ)は現在世界90カ国以上で承認され、治療に使われています。この抗体は、IL-6の信号をブロックすることによりこれら関節リウマチ、若年性特発性関節炎、キャッスルマン病、強皮症、リウマチ様筋痛症、大動脈炎(高安病)など多くの疾患の治療に画期的な効果が発揮されることが報告され、昨年12月のNew England J. of MedicineのEditorialには若年性特発性関節炎の治療に新しい時代が来たと書かれました。
本研究成果が社会に与える影響(本研究成果の意義)
ここで重要な問題が2つあります。1つは何故IL-6の異常産生がこれらの病気をひきおこすのか?という問いかけであり、他の1つは何故IL-6の異常産生が起こるのか?という問題です。
第1の問いかけは、岸本教授はじめ多くの研究者により、IL-6がヘルパーTリンパ球の1つで病気を引き起こすことに直接関わるTh17を作り出すことに必須の分子であるということに始まる一連の研究でその大要が明らかとなりました。
今回の岸本教授らの論文は、第2の問いかけ「何故IL-6の異常産生が起こるのか」に解答を与えるものです (図1) 。
IL-6 mRNAに結合することを防ぐ化合物の開発はIL-6異常産生に起因する炎症性自己免疫疾患の新たなる治療薬の開発につながるでしょう。
特記事項
本成果は、2013年5月13日の午後3時(アメリカ東部時間)に米国科学アカデミー紀要(PNAS)オンライン版に掲載されます。
研究の詳細な説明
当グループは、IL-6RNAの3'非翻訳領域に特異的に結合し、このmRNAの分解を防ぐ分子が存在することを発見した。この分子はIL-6の産生を誘導するシグナルにより同時に誘導され、IL-6RNAが長時間に亘り安定的に存在し、IL-6の異常産生に関わることを証明した。
この分子「Arid5a」を欠損させたマウスではエンドトキシン投与によるIL-6の異常産生とエンドトキシンショックが起こらないこと、又多発性硬化症のマウスモデルにおいてその発症が抑えられることが認められた。
以前に審良静男(IFReC 拠点長)らのグループによりIL-6 mRNAを特異的に破壊する分子(Regnase-1)が発見されているが、今回発見された分子はIL-6 mRNAの3'非翻訳領域でRegnase-1の作用を拮抗的に阻害することが証明された。
正常状態ではIL-6は作られてもすぐに消し去られることが必要であり、Regnase-1はその役割を果たしているが、今回発見されたArid5aはこのRegnase-1の作用を阻害し、IL-6の異常産生、病気の発症につながる可能性が考えられる。
この分子の産生を抑える化合物、あるいはこの分子がIL-6 mRNAに結合することを防ぐ化合物の開発はIL-6異常産生に起因する炎症性自己免疫疾患の新たなる治療薬の開発につながるであろう。
参考図
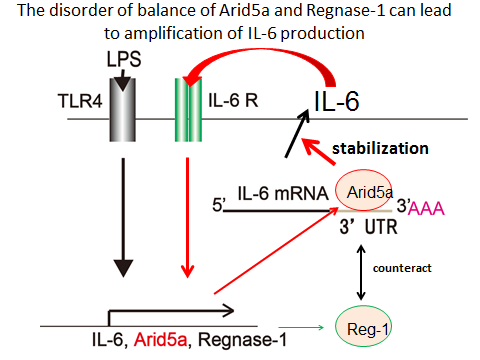
図1 Regnase-1 と Arid5aという分子の働きのバランスが崩れると、IL-6の異常産生が引き起こされる
発表論文
"Arid5a controls IL-6mRNA stability, which contributes to elevation of IL-6 level in vivo"
「Aird5aはIL-6mRNAの安定性をコントロールし、生体内におけるIL-6の上昇に寄与する」
